Монокальций-фосфат
Cтраница 3
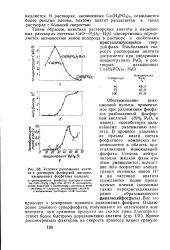 |
Условия разложения апатита в растворах фосфорной кислоты, насыщенных фосфатами кальция. [31] |
Обезвоживание реакционной пульпы, применяемое при разложении фосфатов разбавленной фосфорной кислотой ( 39 % Р2Ь5 и менее), способствует дальнейшему разложению апатита. В процессе удаления из пульпы влаги состав фосфатного комплекса перемещается в область кристаллизации монокальций-фосфата. [32]
 |
Схема производства суперфосфата непрерывным способом. [33] |
Наиболее медленным процессом является дозревание. Ускорить дозревание можно охлаждением суперфосфатной массы и испарением из нее воды, что способствует кристаллизации монокальций-фосфата и повышает скорость реакции ( б) вследствие увеличения концентрации Н3РО4 в растворе. Для этого на складе перемешивают и распыляют суперфосфат. [34]
Фосфат разлагается смесью серной и соляной кислот. Образовавшийся раствор НзРО4 и СаС12 после отделения гипса нагревается, - при этом выделяется газообразный хлористый водород и осаждается монокальций-фосфат. Хлористый водород абсорбируется и снова используется в процессе. [35]
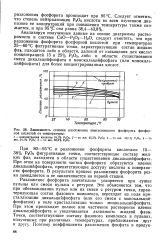 |
Зависимость степени - разложения кингисеппского фосфорита фосфорной кислотой от температуры. [36] |
Разложение фосфорита значительно ускоряется при сушке пульпы или смеси пульпы с ретуром. Это объясняется тем, что при обезвоживании пульп или их смеси с ретуром точка, характеризующая состав фазового комплекса, переходит из поля кристаллизации дикальцийфосфата ( или его смеси с монокальций-фосфатом) в поле кристаллизации только монокальцийфосфата. При этом происходит полное или частичное растворение пленок дикальцийфосфата и увеличивается активность жидкой фазы. Точки, соответствующие составу фазового комплекса в пульпах, полученных при различных температурах, приближаются друг к другу. [37]
В этой главе приводятся результаты некоторых исследований, связанных с изучением возможности получения сложно-смешанных концентрированных удобрений на основе организованных в Советском Союзе и развивающихся производств двойного суперфосфата. Создание совершенных и экономичных способов переработки аммонизированного двойного суперфосфата в сложные удобрения требует дальнейшего изучения условий пересыщения аммонизированных растворов и кристаллизации из них твердых фаз, интенсификации камерного производства двойного суперфосфата, гранулирования сложных удобрений, содержащих монокальций-фосфат, и некоторых других вопросов, которым и посвящены приведенные здесь новые материалы. [38]
На второй стадии реакции разложения фосфата кислотами происходит кристаллизация монокальцийфосфата. Жидкая фаза становится насыщенной по отношению к фосфатам кальция к моменту окончания созревания суперфосфата в камере. Кристаллизация монокальций-фосфата происходит в гелеобразной массе, где процесс разложения оставшейся массы фосфатного сырья идет очень медленно. Поэтому затруднено как создание пересыщения, так и образование твердой фазы. Образование кристаллов монокальцийфосфата происходит в ярко выраженной диффузионной области. Скорость кристаллизации монокальцийфосфата по сути дела лимитируется скоростью разложения сырья фосфорной кислотой. [39]
Гигроскопичность продукта и - его нейтрализация. Суперфосфат с высокой свободной кислотностью ( более 5 % Р2ОВ) при 20 С в тех случаях, когда относительная влажность воздуха составляет 70 - 100 %, поглощает атмосферную влагу. Поглощенная влага растворяет некоторое количество монокальций-фосфата, вызывая его разложение на дикальцийфосфат и фосфорную кислоту. Выделение же дополнительного количества свободной фосфорной кислоты еще больше увеличивает гигроскопичность суперфосфата. [40]
P % Os - Н2О позволяют вычислить для разных условий равновесную степень разложения моно-кальцийфосфата водой. Но пересыщенные растворы [9, 10] яереходят в стабильное равновесие весьма медленно ( стр. Ранее [11] была изучена скорость гидролиза монокальций-фосфата в зависимости от весового отношения соли к воде ( С: В) и от температуры. В присутствии свободной фосфорной кислоты гидролиз монокальцийфосфата при отношении С: В, равном 0 5 - 1 5, при 20 С практически не происходит в течение 6 час, а при 40 С - в течение 1 5 - 2 час. [41]
Раздельное получение односторонних удобрений основано на нейтрализации фосфорной кислоты в азотнокислотной вытяжке известняком или известковым молоком. При этом образуется осадок дикальцийфосфата ( преципитата), который отделяют от раствора фильтрацией и высушивают. Остающийся раствор нитрата кальция выпаривают и кристаллизуют. Возможно также раздельное получение монокальций-фосфата и нитрата кальция ( стр. [42]
Нейтрализацию пульпы проводят в нескольких реакторах, снабженных быстроходными мешалками. В последний реактор вводят только COg. Постепенное повышение рН реакционной массы в нейтрализаторах и ее интенсивное перемешивание предотвращают возможность загустевания пульпы. Установлено, что загустева-ние пульпы обусловлено выпадением в осадок монокальций-фосфата при рН 2 2 - 2 7, а при более высоком рН ( в пределах 5 - 6) - осаждением кремнефторидов. В присутствии даже небольших количеств солей магния и алюминия вязкость реакционной массы также повышается. Процесс нейтрализации протекает с выделением тепла, поэтому пульпу охлаждают водой, поступающей в рубашку реакторов, поддерживая температуру пульпы на уровне 60 - 80 С. [43]
Как уже упоминалось, основная часть серной кислоты потребляется для изготовления удобрений. Для питания растений особенно нужны фосфор и азот. Природные фосфорные соединения ( апатиты и фосфориты) содержат фосфор в виде трудноусвояемого нерастворимого соединения - трикальцийфосфата Са3 ( РО4Ь - При воздействии на апатиты и фосфориты серной кислотой получают кислые соли фосфорной кислоты: дикальцийфосфат СаНР04 - 2Н2О ( преципитат), растворимый в слабых органических кислотах почвы, и монокальцийфосфат Са ( Н2РО4) 2 - Н2О, растворимый в воде. Фосфор растворимых соединений усваивается растениями. Монокальций-фосфат - основная часть удобрения суперфосфата. [44]
Этим различиям в цене соответствует и некоторая разница в условиях применения. Поэтому немаловажно знать, в какой форме действующее вещество входит в состав сложных удобрений. Особенно ценны такие сведения в отношении фосфора, поскольку в этом случае, в зависимости от используемой формы - суперфосфата, дикальцийфосфата, шлаков или фосфоритной муки, сильно колеблется не только стоимость весовой единицы, но и степень растворимости, которая, в свою очередь, требует несколько различных условий применения. Форма фосфорного соединения является важным фактором в оценке сложного удобрения. Особенно высоко ценятся легкорастворимые формы монокальций-фосфата и фосфата аммония. [45]
Страницы: 1 2 3 4