Мономагнийфосфат
Cтраница 2
Вследствие большой растворимости мономагнийфосфата по окончании второй стадии реакции жидкая фаза остается ненасыщенной им - он полностью находится в растворе. Вследствие этого степень нейтрализации фосфорной кислоты оказывается весьма высокой. По этим причинам разложение сырья резко замедляется уже во второй стадии процесса, а скорость его в третьей стадии становится совсем незначительной. В связи с этим, а также потому, что гигроскопичный мономагнийфосфат ухудшает физические свойства суперфосфата из фосфоритов Кара-Тау, целесообразно предварительно обогащать их для удаления некоторой доли соединений магния. [16]
Как и при 25, мономагнийфосфат разлагается водой. [17]
Это объясняется образованием различных кристаллогидратов мономагнийфосфата. Чтобы уменьшить слеживаемость продукта, необходимо ускорять процессы кристаллизации путем сушки суперфосфата ( до влажности 4 %) и его охлаждения посредством распыления и пере-лопачивания. [18]
Превращение сульфата магния при этом в хорошо растворимый мономагнийфосфат, остающийся в растворе, является главной особенностью разложения фосфоритов Каратау и других, содержащих магниевые соединения. [19]
 |
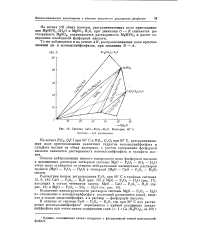
Система MgO - Р305 - Н20. Изотерма 80 С. [20] |
Таким образом, стабильные водные растворы мономагнийфосфата, не выделяющие в донную фазу димагнийфосфата, могут быть получены гораздо более концентрированными, чем аналогичные растворы монокальцийфосфата. [21]
Изучение кинетики растворимости П3В03 в присутствии мономагнийфосфата при 80 показало, что новое соединение образуется через 20 - 22 часа. [22]
 |
Система СаО - Р206 - Н20. Изотерма 80 С. [23] |
С, разграничивающих поля кристаллизации различных гидратов мономагнийфосфата и сульфата магния на обеих изотермах, с ростом содержания фосфорной кислоты снижается растворимость мономагнийфосфата и сульфата магния. [24]
Причиной этого является высокое содержание в продукте мономагнийфосфата, растворимость которого в фосфорной кислоте значительно выше, чем монокальций-фосфата, и поэтому последний высаливается из раствора. Моно-магнийфосфат, растворяясь в фосфорной кислоте, образует с ней буферную смесь, диссоциируя на Mg2 и Н2РО4 -, что подавляет диссоциацию фосфорной кислоты на Н и Н2РО4, и процесс дораз-ложения резко замедляется. Вследствие высокой растворимости магниевых солей понижение температуры не приводит к их кристаллизации и к существенному изменению концентрации фосфорной кислоты и лишь уменьшает скорость ее взаимодействия с фосфатом. Одновременно с разложением фторапатита происходит разложение и других минералов, входящих в состав фосфата. [25]
Во второй стадии сернокислотного разложения фосфоритов Кара-Тау происходит образование мономагнийфосфата, который вместе со свободной фосфорной кислотой переходит в раствор. [26]
В связи с этим, а также потому, что гигроскопичный мономагнийфосфат ухудшает физические свойства суперфосфата из фосфоритов Каратау, целесообразно предварительно обогащать их для удаления некоторой доли соединений магния. [27]
Аммонизированный суперфосфат при охлаждении схватывается, что объясняется изменением гидратности мономагнийфосфата и образованием других кристаллогидратов. [28]
 |
Система MgO - Р2О6 - Н2О. Изотерма 0е. [29] |
В пределах от 29.5 до 58.4 % Р2О5 растворы насыщены четырехводным мономагнийфосфатом, а при более высоких концентрациях фосфорной кислоты в равновесии с растворами находится безводный мономагнийфосфат. [30]
Страницы: 1 2 3 4