Мономагнийфосфат
Cтраница 3
Вследствие инконгруэнтности растворов системы MgO - Р205 - Н20 по отношению к мономагнийфосфату последний разлагается водой, выделяя в осадок димагнийфосфат, а в раствор - фосфорную кислоту. [31]
Вследствие инконгруэнтности растворов системы MgO - Р2О5 - Н2О по отношению к мономагнийфосфату последний разлагается водой, выделяя в осадок димагнийфосфат, а в раствор - свободную фосфорную кислоту. [32]
При титровании смесей Н РО4 и Mg ( H2PO4) 2 вычисленное содержание мономагнийфосфата, в предположении образования димагнийфосфата, хорошо совпадало с действительным содержанием его в контрольной смеси. [33]
Полученная этими авторами изотерма состоит из ветвей насыщения трехводным димагнийфосфатом MgHPO4 ЗН2О и мономагнийфосфатом Mg ( H2PO4) 2 - xH2O, гидратность которого авторами не установлена. Камерон и Белл [4] отметили также, что фосфат магния, более основной, чем димагнийфосфат, существует при 25 в равновесии только с крайне разбавленными относительно Р2О5 растворами. Концентрации этих растворов слишком малы, чтобы их можно было определить сколько-нибудь точно. Как мы увидим далее, результаты Камерона и Белла являются достоверными лишь для ветви насыщения димагнийфосфата. [34]
То же наблюдается и на ветвях АН, разграничивающих поля кристаллизации ди - и мономагнийфосфатов, при движении R - А. [35]
Как и для солей кальция, с увеличением концентрации Р2О5 растворимость димагнийфосфата растет, а мономагнийфосфата - уменьшается ( см. рис. 71), но в отличие от монокальцийфосфат степень разложения водой мономагний-фосфата почти не зависит от температуры. [36]
Как и для кальциевых солей, с увеличением концентрации Р2О5 растворимость ди-магнийфосфата растет, а мономагнийфосфата - уменьшается ( рис. 75), но в отличие от монокальцийфосфата, степень разложения водой мономагнийфосфата почти не зависит от температуры. [37]
 |
Система MgO - Р2О5 - Н2О. [38] |
Для уточнения температуры и состава жидкой фазы в инвариантной точке АЬ %, выше которой те-трагидрат мономагнийфосфата прекращает свое стабильное существование в равновесии с фосфорнокислыми растворами, мы провели соответствующее экспериментальное определение. [39]
Силикаты магния, например форстерит ( Mg2Si04), реагируют с кислотой, образуя переходящие в раствор мономагнийфосфат и диоксид кремния. [40]
Растворимость димагнийфосфата в водных растворах фосфорной кислоты в пределах 25 - 80 остается практически постоянной; растворимость мономагнийфосфата растет с ростом температуры. [41]
Выше этой температуры двухводный мономагнийфосфат прекращает свое стабильное существование в контакте с фосфорнокислым раствором, и ветвь безводного мономагнийфосфата пересекается непосредственно с ветвью димагнийфосфата. [42]
При достаточно высокой степени разложения фосфорита Кара-Тау образующийся в третьей стадии процесса монокаль-цийфосфат высаливается в твердую фазу более растворимым мономагнийфосфатом. Возможно и появление в твердой фазе дикальцийфосфата, особенно при повышенном содержании в фосфате окиси магния. [43]
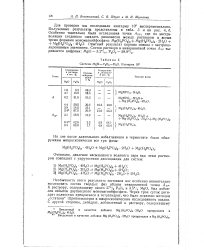 |
Система MgO - Р2О5 - Н2О. Изотерма 10. [44] |
К раствору, содержащему около 57 / 0 Р2О5 и 3.5 / 0 MgO, был добавлен избыток двухводного мономагнийфосфата. Через трое суток диги-драт полностью превратился в тетрагидрат, что было доказано методом остатков Шрейнемакерса и микроскопическим исследованием осадка. [45]
Страницы: 1 2 3 4