Мононитрид
Cтраница 2
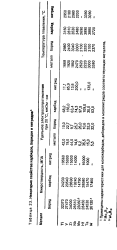 |
Некоторые свойства карбидов, боридое и нитридов1. [16] |
Приведены характеристики для монокарбидов, диборидов и мононитридов соответствующих металлов. [17]
Описана технология изготовления порошков и компактных изделий мононитридов переходных металлов - титана, циркония, ниобия, ванадия и тантала, а также приведены термоэмиссионные свойства и коэффициент излучения до температур порядка 2000 С. [18]
Фазы TaNo80 - 0 до и TaNli00 упоминаются как б - и е-фазы мононитрида, аналогичные соответствующим фазам мононитрида ниобия. В отличие от ниобиевых фаз обе фазы мононитрида тантала имеют гексагональную структуру. В пределах области гомогенности размеры гексагональной элементарной ячейки TaNo s o 9 изменяются от а 2 925 до 2 938 А и от с 2 876 до 2 883 А. Эта 6-фаза имеет структуру WC. Для точки плавления приводятся различные значения, но в среднем tnn 2800 С [14]; при плавлении удаляется азот. [19]
Фазы TaNo80 - 0 до и TaNli00 упоминаются как б - и е-фазы мононитрида, аналогичные соответствующим фазам мононитрида ниобия. В отличие от ниобиевых фаз обе фазы мононитрида тантала имеют гексагональную структуру. В пределах области гомогенности размеры гексагональной элементарной ячейки TaNo s o 9 изменяются от а 2 925 до 2 938 А и от с 2 876 до 2 883 А. Эта 6-фаза имеет структуру WC. Для точки плавления приводятся различные значения, но в среднем tnn 2800 С [14]; при плавлении удаляется азот. [20]
 |
Зависимость температуры перехода в сверхпроводящее состояние ( Тс моноокиси титана стехиометрического состава от концентрации решеточных вакансий в ней. [21] |
Даже при стехиометрическом составе некоторые нитриды имеют заметные концентрации вакансий ( речь идет о двойной дефектности в структуре мононитридов стехиометрического состава TiN, ZrN и HfN), что может влиять на их Тс. Для большинства систем Тс, как правило, уменьшается с понижением содержания неметалла в карбидах и нитридах, и даже для препаратов стехиометрического состава Тс, вероятно, зависит от концентрации вакансий. [22]
При 1870 С навеска оксида алюминия массой 75 82 г полностью реагирует с избытком графита и диазота, образуя монооксид углерода и мононитрид алюминия. Покажите расчетом, что эта реакция термодинамически выгодна в закрытой системе. [23]
Классификация, принятая при рассмотрении ниобиевых сплавов, позволяет сплавы, составы которых лежат на квазибинарной диаграмме левее предельной растворимости монокарбида или мононитрида в молибдене, отнести к дисперсионно-твердеющим, а сплавы с эвтектической кристаллизацией ( доэвтектические) - к дисперсно-упрочненным, или сплавам эвтектического типа. [24]
Позднее Коста и Конте [26], используя несколько иную модель электронных состояний кубических карбидов и нитридов, изучили электронные энергетические спектры монокарбида и мононитрида титана, основываясь на методе сильной связи. При этом, учитывая близость электронных характеристик этих соединений друг с другом и исходного металла ( в данном случае титана), они предположили, что атомы неметалла лишь слабо возмущают электронную структуру тугоплавких соединений, основные черты которых определяются атомами металла. В связи с этим в расчете акцент сделан лишь на влияние d - состояний атомов титана, в то время как перекрывание волновых функций атомов неметаллов и их гибридизация с волновыми функциями металла не учитывались. При проведении расчетов авторы исходили из ионно-ковалентной модели, согласно которой 1 5 электрона атома углерода ( и 2 электрона атома азота) переходят в d - полосу металла. В этом отношении указанная модель аналогична предложенной ранее Уманским [29], по мнению которого в фазах внедрения атомы неметалла частично ( или полностью) отдают свои валентные электроны в s - d - полосу кристалла. Однако в работе Коста и Конте предполагалось также, что электроны несколько оттягиваются к атомам углерода, обусловливая существенную полярность связей. При этом выяснилось, что в рамках использованной модели полосы проводимости TiC и TiN состоят из двух подполос, образованных соответственно из dY - и е-волновых функций атомов металла. [25]
Как уже было указано, титан, цирконий и гафний ( особенно в расплавленном виде) способны интенсивно реагировать с азотом при высоких температурах с образованием рядов твердых растворов, а также нитридов, из которых преимущественную роль играют мононитриды MeN. Нитриды титана, циркония и гафния - кристаллические очень твердые и тугоплавкие металлоподобные вещества. Температуры их плавления соответственно равны 2930, 2950, 3310 С. [26]
Общие погрешности в значениях Ф т при 298 15; 3000 и 6000 К имеют величины порядка 0 01; 0 02 и 0 05 кал / моль-град для одноокиси кремния и 0 02; 0 03 и 0 2 кал / моль-град для мононитрида кремния. [27]
При взаимодействии гидрида урана с рассчитанными количествами аммиака или азота образуются нитриды урана. Светло-серый мононитрид урана устойчив до 1700 С, но подвержен воздействию воздуха и водяного пара. Соединения состава от U2Ns, разлагающегося ч вакууме при 700 - 800 С, до UN2, существующего при высоких давлениях азота, представляют собой монофазные твердые продукты. [28]
Нитрид бериллия бесцветен, очень тверд и тугоплавок: плавится ( под давлением) около 2200 С; при 2240 С без давления) разлагается. Газообразные молекулы мононитрида ( BeN) стойки, по крайней мере до 1500 - 2000 С. [29]
Оксинитриды ниобия не удалось получить нагреванием окислов ниобия с нитридами ниобия или с газообразным азотом. Лишь кубическая б-фаза мононитрида NbN сорбирует небольшое количество кислорода. Кристаллические решетки этих оксинитридов подобны решеткам кубической 6 - NbN или гексагональной e - NbN фаз. Оксинитриды не очень стойки и разлагаются при нагревании до 1000 С. [30]
Страницы: 1 2 3