Поверхностный монослой
Cтраница 2
Для количественной оценки описанных особенностей кинетики реакции требуется знать количество железа, содержащегося в поверхностном монослое. Затем проводят откачку при температуре - 78 С и вновь измеряют изотерму адсорбции окиси углерода при - 196 С. Разность между указанными двумя изотермами соответствует количеству окиси углерода, прочно связанной с поверхностью железа. [16]
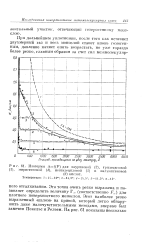 |
Изотермы. t / (. F для лаурпновои ( 2, трлдециловой ( 3, мпристиновой ( 4, поптадецплолой ( 5 п пальмитиновой. [17] |
Эта точка очень резко выражена и позволяет определить величину Г ( соответственно FK) для плотного поверхностного монослоя. Этот наиболее резко выраженный излом на кривой, который легко обнаружить даже малочувствительными методами, впервые был замечен Покельс и Редеем. [18]
Полученные экспериментальные данные свидетельствуют о том, что адсорбция в этих системах идет не в поверхностном монослое, а во всем объеме ультратонких пор. Эти результаты имеют принципиальное значение, подтверждая представления о вырождении поверхности раздела с ростом дисперсности ( стр. Действительно, в рассмотренных примерах уменьшение ач с ростом длины цепи обусловлено не сте-рическими затруднениями, а объемным заполнением; чем больше размер молекулы, тем меньшее число их требуется для заполнения постоянного объема пор. [19]
Следовательно, остается только одно объяснение экспериментальных данных для указанной системы: неприменимость к ней модели поверхностного монослоя. Согласно условию устойчивости ( 1) и формуле ( 2), поверхностный монослой в системе гексан - ацетон является неустойчивым и если бы даже он образовался в какой-то момент, то поверхностный слой стал бы самопроизвольно утолщаться. Мы можем сказать поэтому, что в рассматриваемой системе минимальная возможная толщина поверхностного слоя в исследованном интервале температур составляет около двух монослоев. [21]
В результате получается информация об элементном составе поверхностного слоя ( 1 - 10 атомных слоев под поверхностным монослоем), количестве адсорбированных на поверхности частиц и их природе. [22]
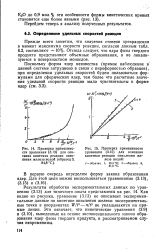 |
Проверка применимости уравнения для описания кинетики реакции окисления железа водой ( образец 3, 84 8 С.| Проверка применимости уравнения для описания кинетики реакции окисления железа водой. [23] |
Отсюда следует, что ядра фазы твердого продукта представляют объемные образования, а не локализуются в поверхностном монослое. [24]
Предельный результат, таким образом, совпадает с результатом, полученным в первом примере: в поверхностном монослое остается лишь компонент с наибольшим временем адсорбции. [25]
Все это, несмотря на простоту метода, говорит о сложности его применения, тем более что поверхностный монослой может состоять не только из плотно-упакованных и вертикально ориентированных молекул красителя, но и содержать в заметных количествах молекулы растворителя и адсорбированные мицеллы растворенного вещества. [26]
Формула ( 2) учитывает конечную скорость собственно адсорбционного процесса, т.е. непосредственного обмена молекулами ПАВ между поверхностным монослоем и прилегающим раствором, связанную с наличием потенциального барьера между ними. В пользу существования такого барьера-говорят измерения скоростей адсорбционных процессов как в случае ионогенных, так и неионогенных ПАВ [ 4 - II ], результаты которых не соответствуют диффузионной кинетике. [27]
В результате должна, очевидно, возникать ситуация, при которой молекулы ПАВ из приповерхностного монослоя, находящиеся рядом с участками поверхностного монослоя, уже занятыми молекулами ПАВ, практически лишены возможности перескочить в поверхностный слой. В этом и состоит смысл дополнительного множителя ( 1 - Г / Т) в первом слагаемом правой части ( 2), описывающем результирующий поток адсорбирующихся молекул. [28]
Выбор модели для обменной структуры никеля и кислорода до некоторой степени зависит от относительных эффективных размеров атомов кислорода и никеля в поверхностном монослое. Вероятно, они не совпадают с размерами внутри кристаллической решетки окиси никеля, поскольку очевидно, что из-за различия в числе ближайших соседей характер связей и электронные переходы в обоих случаях также различаются. Весьма сомнительно, чтобы для поверхностного монослоя кристалла никеля, состоящего из кислородных и никелевых атомов, была применима жесткая сферическая модель. Следует отметить, что фотоэлектрические характеристики такой поверхности соответствуют фаулеровской кривой для металлов, в то время как после образования на поверхности полупроводящего окисла это не должно иметь места. [29]
Интуитивно полагая, что изменение молярных долей в растворе и поверхностном слое должно быть симбатным, БаТлер и Уайтмен объяснили наблюдаемое явление неприменимостью модели поверхностного монослоя к изученной системе и предложили двухслойную модель поверхности с резким различием слоев по составу. Однако наблюдавшиеся экстремумы на изотерме состава поверхностного слоя были слишком слабы для их однозначного объяснения. В работе Гуггенгейма и Адама [38] было предложено другое объяснение тех же самых экспериментальных данных, основанное на предположении о наличии отклонений молярной площади от аддитивности в рамках модели поверхностного монослоя. [30]
Страницы: 1 2 3 4