Монофторид
Cтраница 1
Монофториды обладают нормальной устойчивостью, а полифториды, у которых у одного и того же атома углерода находится более чем один атом фтора, химически инертны. Например асимметрический ди-фторэтилен CH2 CF2 устойчив к окислению воздухом, в отличие от соответствующего дихлорпроизводного, которое в этих условиях легко окисляется. Стабилизирующее влияние атомов фтора распространяется и на атомы других галоидов, находящихся у того же или у соседнего атома углерода. Так, дихлордифторметан CC12F2 совершенно не поддается гидролизу и действию расплавленного натрия. Одно из объяснений инертности полифторидов ( Брокуей, 1937) основывалось на наблюдении, что в то время как длина нормальной связи С-F в монофторидах равна 1 42 А, в полифторидах она уменьшается до 1 35 А Длина связи С - С1 в смешанных хлорполифторидах также меньше нормальной на 0 03 - 0 07 А. Подобное уменьшение длины связи не наблюдается у полихлоридов. [1]
Монофторид получается, в зависимости от условий опыта, переменного состава: черный порошок при составе [ CF0 68 ] по мере увеличения содержания фтора светлеет. При достижении формулы [ CF ] образуется чисто белый и прозрачный для света порошок. [2]
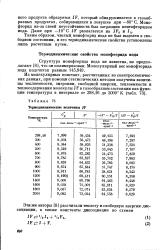 |
Термодинамические величины JF. [3] |
Монофторид из-за своей неустойчивости был загрязнен пентафторидом иода. [4]
Монофториды не проявляют каких-либо аномальных физических свойств по сравнению с обычными алкил - или арилфторсила-нами. В отличие от трифторпроизводных в их ИК-спектрах характеристические частоты карбонильной группы не отличаются от таковых для соответствующих триэтоксисиланов. [5]
 |
Свойства фторидов хлора. [6] |
Монофторид требует для своего распада мало энергии, но так как реакция протекает с неизменным числом молекул, GIF устойчив. [7]
Монофторид углерода не смачивается водой и не реагирует даже с концентрированными кислотами и щелочами. С водородом не реагирует вплоть до 400 С. При быстром нагревании [ CF ] разрушается со вспышкой и дает облако мелкой сажи, а также газообразный CF4 в смеси с высшими фтороуглеродами. [8]
Монофториды триалкилсвинца - самые устойчивые кристаллические галогениды триалкилсвинца; они ядовиты, бесцветны, более растворимы в воде, чем в бензоле, и получаются обработкой гидроокисей триалкилсвинца разб. [9]
Монофторид галлия более устойчив, чем обладающий сильными окислительными свойствами трифторид. [10]
Монофторид таллия ( Т IF) хорошо изучен многочисленными исследователями. [11]
Монофториды насыщенных углеводородов гидро - - лизуются очень легко. Следует отметить, что они более чувствительны к гидролизу концентрированными кислотами, чем концентрированными щелочами. Кислоты действуют одновременно как в направлении омыления, так и отщепления фтористого водорода. [12]
Монофторид углерода CF легко получается при взаимодействии фтора с сопряженной системой связей в решетке графита. При этом возникают гофрированные слои из атомов С [ напоминающие аналогичные слои [111] в решетке алмаза ( ср. С насыщаются атомами F. [13]
Загрязненный примесями монофторид ртути Hg2F, был получен Берцелиусом j31 ] нагреванием тщательно перемешанной смеси Hg2Cl2 и NaF. Более чистое вещество получено [32] растворением свежеосажденного карбоната закиси ртути в плавиковой кислоте. [14]
Итак, твердый монофторид бериллия неустойчив и может мыслиться лишь как термодинамически замороженное вещество. Такое положение является частным случаем общего правила о нестойкости соединений с одновалентным состоянием атомов щелочноземельных металлов. Но это положение отнюдь не означает того, что соединения, подобные BeF, не могут быть вполне устойчивыми нормальными соединениями при высоких температурах, в особенности если эти вещества летучи. В интервале 1500 - 3800 К дифторид при атмосферном давлении устойчив, но при восстановлении его или при значительном понижении давления может терять часть фтора, давая одновременно устойчивый монофторид. [15]
Страницы: 1 2 3 4