Ж-ксилол
Cтраница 2
При окислении ж-ксилола образуется ж-фталевая ( изофта-левая) кислота, которая может быть использована в синтезе алкидных смол; для этой цели пригодны также диметиловые эфиры изофталевой кислоты. Процесс ведут в условиях, аналогичных окислению я-ксилола. [16]
Большая часть ж-ксилола изомеризуется в п - и о-ксилолы, масштабы промышленного применения которых значительно выше, чем лг-изомера. Содержание ж-ксилола во фракциях С8 катализата риформинга и пироконденсата составляет 35 - 45 и 25 - 30 % ( мае. [17]
Окислительным аммонолизом ж-ксилола в присутствии катализаторов - V205 или NH4V03 и As203 - при 380 С получают изофталодинитрил и последующим гидрированием - ж-ксили-лендиамин. Изофталодинитрил применяется в производстве фунгицидов и гуанаминовых смол. Ксилилендиамин используется в синтезе красителей и лекарственных веществ. [18]
В случае ж-ксилола наблюдается более быстрое уменьшение количества ж-ксилола в ксилольных фракциях. Таким образом, даже в присутствии вдвое большего количества хлористого алюминия изомеризационные процессы п - и о-ксилолов легко обнаруживаются в реакции метилирования. Это говорит о том, что первичное вступление метальных групп в метаположение не должно затемняться процессами изомеризации. [19]
Установка выделения ж-ксилола экстракцией смесью HF - f BF8 сооружена в Мицухиме ( Япония) фирмой Japan Gas Chemical Go. В комплекс, помимо этой установки, входят установки изомеризации и выделения этилбензола, о - и га-ксилола ( см. гл. [20]
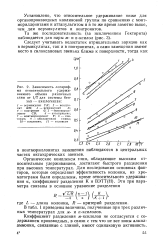 |
Зависимость логарифма относительного удерживаемого объема различных глин от 1 / Т для системы бензол - циклогексан. [21] |
Коэффициент разделения ж-ксилолов не согласуется с содержанием производных, в связи с тем что не все ионы алкил-аммония, связанные с глиной, имеют одинаковую активность. [22]
Как из ж-ксилола и метилянтарной кислоты получить 1 2 7-триметил - 4-метоксинафталин. [23]
В пирогенезитах ж-ксилола вдвое или втрое больше, чем re - ксилола, а о-изомер не превышает 5 - 10 % их суммы. [24]
При окислении ж-ксилола при 160 С и 1 5 - 2 МПа в присутствии ацетата марганца и бромида кобальта получают изо-фталевую кислоту. Процесс проводят в растворе уксусной кислоты. [25]
При окислении ж-ксилола при 160 С и 1 5 - 2 МПа в присутствии ацетата марганца и бромида кобальта получают изофтале-вую кислоту. Процесс проводят в растворе уксусной кислоты. [26]
Газофазное окисление ж-ксилола не представляет практического интереса, так как приводит к преимущественному образованию малеинового ангидрида и диоксида углерода. [27]
При окислении чистого ж-ксилола получают 99 % - ную изофталевую кислоту. [28]
В противоположность ж-ксилолу в ароматической фракции Се этот углеводород С9 можно сравнительно легко выделить ректификацией. [29]
Получаемый описанным способом ж-ксилол имеет чистоту 98 8 % ( мол. Изменяя условия процесса, в частности, увеличивая продолжительность взаимодействия фтористого водорода и трехфтористого бора с ароматическими углеводородами, можно влиять на изомеризацию ксилолов и таким спосооом управлять соотношением получаемых изомеров ксилола. Для увеличения выхода - ксилола предусматривают специальную стадию изомеризации, используя в качестве изомеризующего средства тот же реагент HF BF3 ( см. гл. Процесс характеризуется компактностью оборудования и сравнительно невысокими капитальными затратами, несмотря на то, что отдельные узлы оборудования выполнены из дорогих материалов. [30]
Страницы: 1 2 3 4