Автокатализ
Cтраница 2
Автокатализом является превращение, которое ускоряется веществами, образующимися в самой реакции. Так как количество продуктов реакции непрерывно увеличивается, автокаталитический процесс характеризуется постоянным нарастанием константы скорости реакции. [16]
Автокатализом называют процесс изменения скорости химической реакции, при которой катализатор не вводится извне, а является одним из продуктов данной реакции. [17]
Тогда автокатализ может развиться, несмотря на то. [18]
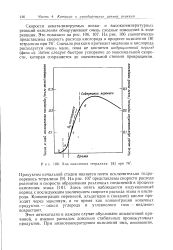 |
Ход окисления тетралина 18 ] при 76. [19] |
Этот автокатализ в каждом случае обусловлен аналогичной причиной, а именно распадом довольно стабильных промежуточных продуктов. [20]
Этот асимметрический автокатализ макромолекул имеет глубокую аналогию с ферментативными асимметрическими синтезами в природе. [21]
Примером автокатализа может служить растворение меди в азотной кислоте; при этом катализатором является образуемый в результате реакции оксид азота. Другим примером автокатализа может служить реакция взаимодействия перманганата калия в сернокислой среде со щавелевой кислотой или ее солями ( уравнение реакции см. стр. Образующиеся в результате реакции ионы марганца Мп2 катализируют реакцию. Эта реакция широко используется в качественном и количественном анализе. [22]
 |
Зависимость стандартных окислительно-восстановительных потенциалов восстановителей от рН раствора при 25 С. [23] |
Степень автокатализа зависит и от природы металла, и от природы восстановителя. [24]
Степень автокатализа зависит от природы металла и восстановителя. [25]
Примером автокатализа может служить растворение меди в азотной кислоте; при этом катализатором является образуемый в результате реакции оксид азота. Другим примером автокатализа может служить реакция взаимодействия перманганата калия в сернокислой среде со щавелевой кислотой или ее солями ( уравнение реакции см. с. Образующиеся в результате реакции ионы марганца Мп2 катализируют реакцию. Эта реакция широко используется в качественном и количественном анализе. [26]
Примером автокатализа может служить растворение меди в азотной кислоте, при этом катализатором является образуемый в результате реакции окисел азота. Другим примером автокатализа может служить реакция взаимодействия перман-ганата калия в сернокислой среде со щавелевой кислотой или ее солями ( уравнение реакции - см. стр. Образующиеся в результате реакции ионы двухвалентного марганца Мп катализируют реакцию. Эта реакция широко используется в качественном и количественном анализе. [27]
Причины автокатализа и механизм процессов химического осаждения ( восстановления) металла тоже еще полностью не раскрыты. Существует довольно много различных предположений, среди которых можно выделить два направления. [28]
Степень автокатализа зависит от природы металла и восстановителя. [29]
Причины автокатализа и механизм процессов химического осаждения ( восстановления) металла тоже еще полностью не раскрыты. Существует довольно много различных предположений, среди которых можно выделить два направления. [30]
Страницы: 1 2 3 4