Пассивное железо
Cтраница 1
Пассивное железо переходит в раствор в виде трехвалентных ионов. [1]
Пассивное железо не растворяется в слабых кислотах, не осаждает Си и Ag из их солей. [2]
Пассивное железо не вытесняет медь из растворов ее солей. Активный хром посылает в раствор ионы Сг34, пассивный - ионы СгО; аналогично ведет себя марганец. [3]
Если пассивное железо, внешне не отличающееся от обычного железа, поцарапать по поверхности твердым предметом, то оно начинает растворяться в кислотах. Это показывает, что на поверхности железа существует какая-то пленка, защищающая железо от действия кислот и препятствующая растворению его при электролизе. [4]
 |
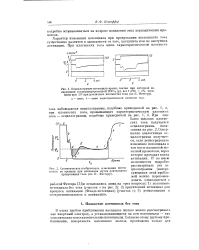
О. Анодные поляризационные кривые для хрома в растворе 1 н. НС1 СНзОН с различными добавками воды ( %. 1 - О. 2 - 1. 3 - 2. 4 - 3. 5 - 4. 6 - 5. 7 - 10. [5] |
Снижение скорости растворения пассивного железа в присутствии окислителей может быть связано с их участием в образовании пассивирующего слоя на металле. [6]
 |
Кривые потенциал - время при активации током и самопроизвольной репассивации железа в 12 н. растворе HN03 ( по Бонгофферу и Феттеру 1в4. [7] |
С помощью катодного тока пассивное железо в азотной кислоте может активироваться. Однако через короткое время ( порядка секунд), несмотря на продолжающуюся катодную поляризацию, наступает самопроизвольная репассивация, которая через определенное время при непрерывном пропускании катодного тока сменяется активацией. На рис. 364 приведены типичные кривые потенциал - время для активации катодным током с самопроизвольной репассивацией. Ниже на рис. Зббг будет показано несколько подобных циклов при непрерываемом катодном токе. [8]
В очень грубом приближении пассивное железо можно рассматривать как инертный электрод, а устанавливающиеся на нем потенциалы - как окислительно-восстановительные потенциалы. [10]
Если хром, нержавеющие стали, пассивное железо поляризовать катодно, то их пассивность нарушается. Это происходит в результате восстановления пассивирующего окисла или адсорбционной кислородной пленки. Кроме того, согласно адсорбционной теории, атомы водорода, разряжающиеся на переходных металлах, стремятся раствориться до некоторой степени в самом металле. Этот растворенный водород частично диссоциируется на протоны и электроны, причем электроны способны заполнить вакансии в d - уровне металла. Следовательно, переходный металл, содержащий достаточное количество водорода, больше не способен хемосорбировать кислород или становиться пассивным, так как d - связь уже заполнена. [11]
По адсорбционной теории, наблюдаемый Фладе-потенциал пассивного железа слишком положителен ( примерно на 0 6 в), чтобы его можно было объяснить существованием каких-либо окислов железа в равновесии с железом. [12]
 |
Изменение потенциала железного электрода в процессе его самопроизвольного активирования в 1 N H2SOi, наступающего после выключения анодного поляризующего тока. [13] |
Фладе [1] обнаружил, что активирование пассивного железа в кислых растворах сопровождается характерным изменением его потенциала. [14]
В заключение можно утверждать, что поведение пассивного железа в кислых растворах типично для физико-химической системы, характеризующейся появлением нестабильного состояния. [15]
Страницы: 1 2 3 4 5