Окисное железо
Cтраница 1
Окисное железо определяют в свежевзятой пробе. Спустя несколько часов результаты определения уже будут завышенными. [1]
Окисное железо обесцвечивают восстановлением его в за-кисное добавлением металлического алюминия или раствора гидроксиламина. [2]
 |
Содержание железа в некоторых породах и минералах. [3] |
Окисное железо часто связано с алюминием, а закисное железо - с магнием. [4]
Окисное железо восстанавливают в закисное добавлением отходов железа; раствор осветляют добавкой желатина или путем осаждения сернистых соединений. Ни в коем случае не следует фильтровать раствор без предварительной коагуляции содержащихся в нем в виде суспензии неразложившихся частиц. После фильтрования молекулярное отношение 5О4 / ТЮ2 в растворе без учета сульфата закисного железа составляет от 1 до 2, и раствор может рассматриваться как кислый раствор титанил-сульфата. [5]
Окисное железо найдено в таких морских осадках, образовавшихся около 2 7 млрд. лет тому назад. [6]
Окисное железо экстраги-тся наилучшим образом при рН чуть ниже / Н гидролиза. [7]
Окисное железо экстрагирующееся хуже, чем молибден, мож ( быть вытеснено из органической фазы молибденом. Вольфра экстрагируется слабо, а экстрагированный кобальт вытесняете железом и молибденом. Никель, трехвалентный хром, свине и пятивалентный ванадий не экстрагируются. [8]
Хлористое, сернокислое окисное и азотнокислое окисное железо можно получить, растворяя металлическое железо при нагревании соответственно в соляной, серной или азотной кислоте. Выпавшие кристаллы отфильтровывают и высушивают при 25 - 30 С в струе углекислого газа или азота. [9]
Пикрат окисного железа, высушенный при 100, по своей чувствительности несколько превосходит перекристаллизованный тетрил. [10]
Восстановление окисного железа в закисное. Если почва насыщена водой, в ней происходят процессы восстановления железа, приводящие к оглеению почвы. Роль микроорганизмов в восстановлении железа может быть двоякой: 1) восстановление железа может быть результатом накопления восстановленных продуктов ( H2S, H2 и СН4), выделяющихся в процессе брожения, реагирующих с окисным железом; 2) восстановление железа может быть и результатом непосредственного воздействия специфичной группы микроорганизмов на окисное железо, подобно процессу денитрификации, имеющей для них энергетическое значение. [11]
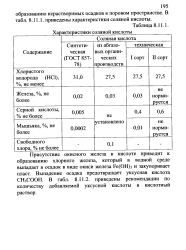 |
Характеристики соляной кислоты. [12] |
Присутствие окисного железа в кислоте приводит к образованию хлорного железа, который в водной среде выпадает в осадок в виде окиси железа Ре ( ОН) з и закупоривает пласт. В табл. 8.11.2. приведены рекомендации по количеству добавляемой уксусной кислоты в кислотный раствор. [13]
Хлорид окисного железа вызывает появление фиолетового окрашивания, исчезающего от избытка реактива вследствие окисления. [14]
Комплексы окисного железа распадаются на два основных класса. Некоторые комплексы, как Fe ( H2O) и FeFI, обладают высокими парамагнитными моментами, указывающими на наличие пяти неспаренных электронов; другие комплексы, как, например, Fe ( CN) e -, имеют гораздо меньшие моменты, соответствующие одному неспаренному электрону. Полинг первоначально предположил, что комплексы первого типа являются в основном ионными с пятью З - орбитами иона Fe3, занятыми неспаренными электронами по одному на каждой орбите, и с ли-гандами, которые удерживаются электростатическими или ионно-дипольными силами. Комплексы типа феррициани-да рассматривались при этом как ковалентные. [15]
Страницы: 1 2 3 4