Накопление - продукт - реакция
Cтраница 1
Накопление продуктов реакции в каждой точке стеклопластика определяется произведением константы скорости реакции на концентрацию среды. Химические реакции, сопровождающие массопередачу, значительно осложняют оценку проницаемости стеклопластиков. [1]
Накопление продуктов реакции ( метана и атомарного водорода, рекомбинирующегося в молекулы) происходит первоначально в порах и микропустотах в приграничных объемах зерен металла труб ОТ и НКТ. По границам зерен концентрируются атомы примесей и пустоты, создаются приграничные сегрегации С, Si, Mn и особенно серы, в результате чего граничные участки зерен обогащаются также и углеродом. Кроме того, границы зерен в энергетическом отношении являются метастабильными. [2]
Однако накопление продуктов реакции - олефинов, содержащих сопряженную с двойной связь С - С, резко облегчает инициирова-ние цепей. В результате уже при небольшой глубине крекинга цепной процесс, при котором цепи инициируются при распаде первичных продуктов термических превращений циклопарафинов, становится быстрее реакции, протекающей через бирадикал, и в начальных стадиях реакция самоускоряется. [3]
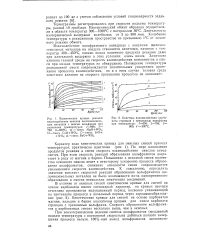
Кинетика накопления продуктов реакции при различных температурах и выбор оптимального режима окисления рассматриваются ниже. [4]
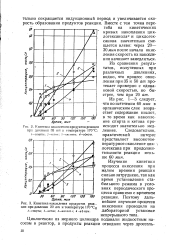 |
Кинетика накопления продуктов реак. ции при давлении 20 am и температуре 170 С. [5] |
Кинетика накопления продуктов реакции давлении 35 am и температуре 170 С: - спирты; 2-кетон; 3-кислоты; 4-эфиры. [6]
На скорость накопления продуктов реакции при определенной температуре изменение давления влияет незначительно. Как видно из рис. 4 - 6, снижение давления несколько снижает концентрацию кислот, почти не влияя на скорость накопления спиртов. [7]
По мере накопления продуктов реакции в смеси скорость взаимодействия окислов замедляется. При этом скорость реакций образования вольфраматов возрастает в ряду от магния к барию. Повышение в исходной смеси количества основного окисла ведет к некоторому ускорению процесса образования вольфраматов; снижение основности смеси сопровождается уменьшением скорости взаимодействия. [9]
По мере накопления продуктов реакции, ускоряется их вымывание из аппарата; в конце концов, скорости образования и вымывания продуктов уравниваются, и концентрация продуктов в аппарате достигает стационарного значения. [10]
На скорость накопления продуктов реакции при определенной температуре изменение давления влияет незначительно. Как видно из рис. 4 - 6, снижение давления несколько снижает концентрацию кислот, почти не влияя на скорость накопления спиртов. [11]
По мере накопления продуктов реакции D и Е концентрации их увеличиваются; следовательно, скорость обратной реакции и, постепенно увеличивается. [12]
По мере накопления продуктов реакции D и Е концентрация их растет; следовательно, скорость обратной реакции г2 постепенно увеличивается. [13]
Рассмотрим кинетическую кривую накопления продукта реакции. [14]
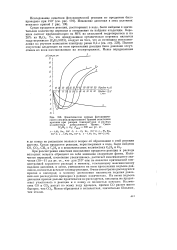 |
Кинетические кривые фотохимического сенсибилизированного бромом окисления, пропана при разных температурах и разных количествах добавленного брома. Смесь 2С3Н8 О2. / нач 300 мм рт. ст. [15] |
Страницы: 1 2 3 4