Общее железо
Cтраница 1
Общее железо в Н3Р04 определяют по реакции Fe2 с о-фенантролином фотометрическим методом. NHdOH до рН 5 - 6, добавляют 10 % - ный раствор солянокислого гидроксиламина, выдерживают 15 мин. ФЭК-М при 500 - 540 нм относительно раствора контрольного опыта. Продолжительность проведения анализа - 2 5 час. [1]
Общее железо в марганцевых рудах определяют из навески 1 - 2 г, как и в железных рудах ( стр. [2]
Общее железо в хромовых рудах определяют бихроматным методом после предварительного удаления из навески хрома. Для этой цели навеску хромита разлагают сплавлением с перекисью натрия или спеканием со смесью карбоната натрия и окиси магния. В результате весь хром окисляется в шестивалентный и образует щелочной хромат, который выщелачивают горячей водой и отделяют фильтрованием. [3]
Общее железо, растворимое в кислоте. [4]
Содержание общего железа вычисляют ш формуле, приведенной на стр. [5]
Содержание общего железа в пересчете на Fe203 вычисляют по формуле, приведенной на стр. [6]
Содержание общего железа в карбонатных породах можно определить таким же методом, который применяется при определении железа в силикатах, только на начальной стадии разложения достаточно выпаривания пробы досуха с соляной кислотой. Растворив остаток в разбавленной соляной кислоте, можно выделить нерастворимый материал и разложить его сплавлением с небольшим количеством безводной соды. [7]
Для определения общего железа оксид и гидроксид железа растворяют в соляной кислоте. Магнетит FeO - Fe203, гетит Fe203 - H20, ле-пидокрокит FeO ( OH) и лимонит 2Fe203 - 4H20 растворяют в соляной кислоте, иногда в присутствии хлорида олова ( II), или металлического алюминия. [8]
При определении общего железа в начале растворения добавляют 0 1 г фтористого натрия ( 32) или навеску спекают, как описано выше. [9]
При определении общего железа, связанном с восстановлением, между газовой горелкой и соседней раковиной помещают для удобства баллон с углекислым газом, снабженный резиновой трубкой. После кипячения и восстановления колба может охлаждаться под краном без перерыва тока углекислоты. Баллон, прикрепленный в вертикальном положении полоской кожи или ткани к краю стойки, должен быть снабжен точным регулирующим приспособлением. Помимо восстановления железа, подобное устройство пригодно для вытеснения двуокиси серы после восстановления ванадия и для приготовления свободной от воздуха воды, насыщенной борной кислотой, для определения закисного железа. [10]
До определения общего железа должна быть удалена сероводородом в виде сульфида платина, внесенная в результате разрушения тигля во время сплавления; иначе сернистая платина вступит в реакцию с перманганатом калия и обусловит завышенный результат титрования и соответственно высокую величину железа. Раствор переливают в полулитровую промывную колбу из стекла пирекс, снабженную притертой стеклянной пробкой, доводят до кипения и в течение 5 мин. Платина за это время осядет в виде черного сульфида; его отфильтровывают и фильтр 3 раза промывают водой, свеженасыщенной сероводородом. [11]
Титриметрическое определение общего железа предусматривает перевод всего имеющегося в образце железа в одно и то же валентное состояние и последующее титрование, в процессе которого валентность железа меняется. Титрование окисных ионов железа никогда не было общераспространенным, и наиболее широко используются методы, в которых закисное железо при титровании переходит в окисное. [12]
Для определения общего железа при концентрациях О О5 - О 2 мг / л применяется колориметрический родановый метод. Реакция протекает в присутствии персульфата аммония в кислой среде. Колориметрирование проводится в цилиндрах Генера Окисное железо определяется тем же путем, что и общее, но без добавления персульфата аммония, - а за-кисное - по разности общего и окисного. [13]
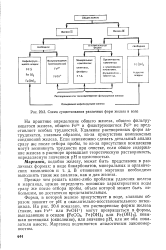 |
Схема существования различных форм железа в воде. [14] |
На практике определение общего железа, общего фильтрующегося железа, общего Fe2 и фильтрующегося Fe2 не представляет особых трудностей. Удаление растворенных форм затрудняется, главным образом, из-за присутствия комплексных соединений железа. Если невозможно сделать детальный анализ сразу же после отбора пробы, то из-за присутствия комплексов могут возникнуть трудности при очистке, если общее содержание железа в растворе превышает теоретическую растворимость, определяемую значением рН и щелочностью. [15]
Страницы: 1 2 3 4