Наличие - внутримолекулярная водородная связь
Cтраница 1
Наличие внутримолекулярной водородной связи и хелатной структуры подтверждается еще и тем, что температура кипения енольной формы ацетоуксусного эфира ниже, чем кетонной. Обычно спирты, молекулы которых образуют межмолекулярные водородные связи, имеют температуры кипения несколько выше, чем карбонильные соединения с таким же числом атомов углерода. [1]
Наличие внутримолекулярной водородной связи в моноанионе ма-леиновой кислоты приводит к его дополнительной стабилизации. Так как этот моноанион является конечным состоянием для первой ступени диссоциации и исходным для второй ступени, то стабилизация приводит к соответствующему увеличению Kai и уменьшению / Са 2 - Это особенно заметно при сопоставлении / СаД и / Cai2 для фумаровой кислоты, в которой внутримолекулярная водородная связь невозможна в результате транс-положения карбоксильных групп. [2]
Наличие внутримолекулярной водородной связи легко установить путем рассмотрения инфракрасных спектров и спектров комбинационного рассеяния света; при этом удается установить и характер водородной связи. [3]
Наличие внутримолекулярной водородной связи в перечисленных соединениях и им подобных было в последнее время доказано спектроскопическими наблюдениями. Изучение инфракрасных спектров, обязанных своим происхождением колебаниям атомов и атомных групп, дало возможность установить, что у всех гидроксильных производных при волновом числе1 около 7100 см-1 наблюдается характерный максимум поглощения. Однако именно в тех веществах, в которых следует допустить наличие внутримолекулярной водородной связи с участием гидроксильной группы, максимум при 7100 см-1 отсутствует. Пики при указанной частоте в инфракрасном спектре были отмечены для m - нитрофенола, для о-крезола, для о-хлорфенола, для гидрохинона, но их не оказалось в спектрах о-нитрофенола, салицилового альдегида, метилсалицилата, 1 5-ди-оксиантрахинона и ацетилацетона. [4]
Наличие внутримолекулярной водородной связи объясняет и очень незначительное изменение цоо перкислот в СС1 при изменении концентрации перкислот. [5]
Наличие внутримолекулярной водородной связи и хелатной структуры подтверждается еще и тем, что температура кипения енольной формы ацетоуксусного эфира ниже, чем кетонной. Обычно спирты, молекулы которых образуют межмолекулярные водородные связи, имеют температуры кипения несколько выше, чем карбонильные соединения с таким же числом атомов углерода. [6]
Наличие внутримолекулярной водородной связи в различных изомерах замещенных фенола впервые было замечено Ауэрсом и Ортоном [10] при исследовании величины молекулярного веса этих продуктов в растворах различной концентрации. Анализируя данные вышеуказанных исследований, можно установить, что при наличии внутримолекулярной связи между гидроксилъной группой фенола и второй функциональной группой в бензольном ядре молекулы вещества обладают малой полярностью, явления ассоциации в разбавленных растворах не наблюдаются и результаты определения молекулярного веса криоскопическим методом в разбавленных растворах совпадают с теоретически подсчитанными. С повышением концентрации раствора заметно увеличивается расхождение между экспериментальными и теоретически рассчитанными данными. Если электронофильная замещающая группа пространственно отдалена от гидроксильной, то происходит уменьшение силы внутримолекулярной водородной связи и молекула ведет себя в растворе как полярная частица. Результатом этого является установленное расхождение между экспериментальными и теоретическими данными определения молекулярного веса даже в сильно разбавленных растворах. [7]
Наличие внутримолекулярной водородной связи легко установить путем рассмотрения инфракрасных спектров и спектров комбинационного рассеяния света; при этом удается установить и характер водородной связи. [8]
Показано, что наличие внутримолекулярной водородной связи существенно сказывается на оптических характеристиках изученных соединений. [9]
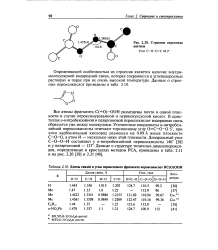 |
Строение пероксида ацетила.| Длины связей и углы пероксидного фрагмента пероксикислот RC ( O OOH. [10] |
Определяющей особенностью их строения является наличие внутримолекулярной водородной связи, которая сохраняется в углеводородных растворах и парах при не очень высокой температуре. [11]
Необычную летучесть енола связывают с наличием внутримолекулярной водородной связи, образующей так называемое хелатное кольцо ( греч. [12]
Данные ИК - и ЯМР-спектооскопии подтверждают наличие внутримолекулярной водородной связи в еноле. Положение равновесия для 1 3-дикетонов и 1 3-кетоэфиров в значительной степени зависит от природы растворителя. Протонные растворителн разрушают внутримолекулярную водородную связь в еноле за счет образования межмолекулярной водородной связи. Более полярная кето-форма, наоборот, стабилизируется с помощью водородной связи с полярными молекулами воды или спирта. В результате доля енола в водном растворе снижается до 23 % для ацетилацетона и до 6 % для ацетоуксусного эфира. [13]
В апротонных средах, наоборот, наличие внутримолекулярной водородной связи играет роль. Благодаря внутримолекулярной водородной связи восстановлению хиноидной группировки предшествует ее автопротонизация ( квазипротонизация), что и приводит к существенному сдвигу потенциалов полуволн в положительную сторону у оксиантрахинонов по сравнению с антрахино-ном. [14]
Таутомерное превращение формазанов происходит чрезвычайно легко, поскольку наличие внутримолекулярной водородной связи облегчает перенос протона в хелатном цикле, поэтому разделить таутомеры не удается. Хелатные циклы симметричных формазанов отличаются большой выравненностью связей. [15]
Страницы: 1 2 3 4