Нарушение - равновесное распределение
Cтраница 1
Нарушение равновесного распределения по внутренним состояниям молекулы в реакции типа ( 5) обязано малой скорости активации по сравнению со скоростью мономолекулярного превращения активной молекулы. Макроскопическим проявлением этого нарушения является уменьшение константы скорости реакции ( 5) с уменьшением давления газа теплового резервуара. [1]
Нарушения равновесного распределения в химических реакциях могут быть обусловлены двумя причинами. Первая состоит в том, что в химической реакции расходуются наиболее богатые энергией частицы, что сильнее всего проявляется в эндотермических реакциях, например в реакциях диссоциации. В тех случаях, когда скорость распада превышает скорость регенерирования активных молекул, распределение колебательной энергии будет отличаться от равновесного и скорость распада становится меньше равновесной. Вторая причина - выделение энергии в элементарных экзотермических актах, которая, вообще говоря, распределяется неравновесным образом по различным степеням свободы реагентов. [2]
Нарушения равновесного распределения энергии в результате химической реакции могут быть обусловлены двумя причинами. Первая из них заключается в уменьшении концентрации наиболее богатых энергией молекул, потребляемых реакцией. Это наиболее ярко проявляется в эндотермических процессах, в частности, в процессах диссоциации, приводящих к уменьшению концентрации молекул на высоких колебательных уровнях. [3]
Нарушение равновесного распределения конформаций приводит к ориентации, максимальной степени которой соответствует область наименьшей ньютоновской вязкости. [4]
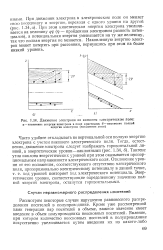 |
Движение электрона во внешнем электрическом поле. [5] |
Рассмотрим некоторые случаи нарушения равновесного распределения носителей в полупроводнике. Кроме уже рассмотренной нами генерации пар носителей в объеме, важное значение имеет введение в объем полупроводника неосновных носителей. [6]
Второй причиной, приводящей к нарушению равновесного распределения энергии в ходе химической реакции, является выделение энергии, распределяющейся между молекулами продуктов реакции. Эта причина наиболее существенное значение имеет в случае экзотермических процессов. [7]
Второй причиной, приводящей к нарушению равновесного распределения энергии в ходе химической реакции, является выделение энергии, распределяющейся между молекулами продуктов реакции. Эта причина наиболее существенное значение имеет в случае экзотермических процессов. Суммарное количество выделяющейся энергии равно энергии активации данного элементарного ( экзотермического) процесса Е0 плюс теплота реакции Q, Еп Q. Выделяющаяся энергия превращается в энергию поступательного движения ЕПОСТ и внутреннюю энергию Л Ш1 продуктов реакции. Впервые явное указание на существование значительных неравновесных аффектов было получено при исследовании мономолокулярных реакций в области низких давлений, где переход от реакции первого порядка ко второму является следствием нарушения равновесного распределения реагирующих молекул по состояниям в области энергий, близких к энергии активации. [8]
В более сложных случаях следует учитывать нарушение равновесного распределения по колебательным и вращательным степеням свободы, а иногда - и по поступательным. При этом, как уже отмечалось ранее, следует учитывать то, что соотношение между макроскопическими временами трел и Треак далеко не всегда определяет степень неравповесности системы. Правильный критерий степени нарушения равновесного распределения, вызываемого реакцией, формулируется в терминах микроскопических констант скоростей релаксации и реакции, определяющих соотношение между скоростями изменения заселенности заданного квантового состояния реагентов за счет этих двух процессов. Именно поэтому изучение элементарных констант релаксационных процессов представляет большой интерес для химической кинетики. [9]
Энергетической накачкой в квантовой электронике называют процесс нарушения равновесного распределения частиц по энергетическим состояниям под воздействием внешнего электромагнитного излучения. Метод энергетической накачки применяется для систем частиц, обладающих тремя и более энергетическими уровнями. [10]
Как правило, нарушение электрохимического равновесия сопровождается нарушением равновесного распределения электрохимически активных частиц между призлектродным пространством и объемом раствора. В этом случае материал электрода служит катализатором реакции между окислительно-восстановительными системами. Поэтому при решении вопроса о природе потенциала следует исследовать каталитические свойства материала электрода. [11]
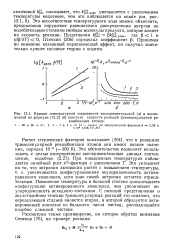 |
Кривые температурной зависимости экспериментальной ( а и вычисленной по формуле ( б констант скорости реакций тримолекулярной рекомбинации атомов. [12] |
Это несоответствие температурного хода можно объяснить, предположив нарушение равновесного распределения энергии по колебательным степеням свободы молекулы продукта, которое влияет на скорость реакции. [13]
Следует отметить, что полученная в выражении (19.9) отрицательная температурная зависимость предэкспоненциального множителя является следствием нарушения равновесного распределения по колебательным состояниям ниже границы диссоциации, причем независимо от величины Ь оно захватывает область ширины kT вблизи границы диссоциации. Нарушение распределения такого типа не получается в теории Крамерса. [14]
Отмечается, что выполнение закона действия масс является необходимым, но не достаточным критерием малости нарушения равновесного распределения реагирующих молекул по степеням свободы. [15]
Страницы: 1 2 3 4