Поверхностное натяжение - водный раствор
Cтраница 1
 |
Понижение поверхностного натяжения в водных растворах жирных кислот ( 15 С. [1] |
Поверхностное натяжение водных растворов всегда отличается от поверхностного натяжения чистой воды. Растворение неорганических солей несколько повышает поверхностное натяжение, тогда как растворение органических веществ - мыла, детергенты, спирты, жирные кислоты - обычно вызывает значительное понижение поверхностного натяжения. Вещества второй группы называются поверхностноактивными. [2]
Поверхностное натяжение водных растворов всегда отличается от поверхностного натяжения чистой воды. При растворении неорганических электролитов - кислот, щелочей, солей - поверхностное натяжение несколько повышается. [3]
Поверхностное натяжение водных растворов всегда отличается от поверхностного натяжения чистой воды. Растворение неорганических солей несколько повышает поверхностное натяжение, тогда как растворение органических веществ - мыл, спиртов, жирных кислот - обычно вызывает значительное понижение поверхностного натяжения. Вещества второй группы принято называть поверхностно-активными. [4]
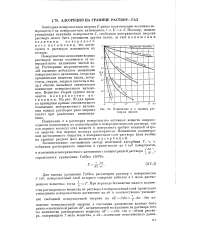 |
Понижение а в водных растворах кислот. [5] |
Поверхностное натяжение водных растворов всегда отличается от поверхностного натяжения чистой воды. Растворение неорганических солей вызывает небольшое повышение поверхностного натяжения, тогда как органические вещества ( мыла, детергенты, спирты, жирные кислоты и мн. Вещества второй группы называются поверхностно активными. На рис. 90 для примера приведены кривые относительного понижения поверхностного натяжения водных растворов ряда жирных кислот при различных концентрациях. [6]
Поверхностное натяжение водных растворов всегда отличается от поверхностного натяжения чистой воды. Растворение неорганических солей несколько повышает поверхностное натяжение, тогда как растворение органических веществ - мыл, спиртов, жирных кислот - обычно вызывает значительное понижение поверхностного натяжения. Вещества второй группы принято называть поверхностно-активными. [7]
Поверхностное натяжение водных растворов ПВС зависит прежде всего от содержания и распределения звеньев ВА в цепях полимера ( см. раздел 1.3), оно уменьшается с ростом концентрации раствора и температуры. Растворы низкомолекулярного ПВС имеют меньшее поверхностное натяжение, чем растворы высокомолекулярного полимера. На поверхностное, натяжение растворов ПВС влияет также степень кристалличности полимера, что позволяет методом вспенивания растворов получать фракции ПВС с различной кристалличностью. [8]
Поверхностное натяжение водных растворов ПАВ резко уменьшается с ростом концентрации вплоть до ККМ, а затем остается постоянным. Преимущество этого метода определения ККМ заключается в том, что точность определения положения точки перегиба ( и, следовательно, ККМ) почти одинакова для веществ с длинной и короткой цепями, так как поверхностное натяжение изменяется во всех случаях практически на одну и ту же величину, С другой стороны, точность других методов, основанных на измерениях электропроводности, показателя преломления, осмотического давления, парциального молярного объема и др., уменьшается почти обратно пропорционально значениям ККМ. [9]
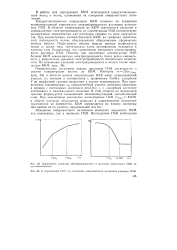 |
Зависимость удельной электропроводности и раствора ионогенного ПАВ от его концентрации.| К определению KKJV, по изменению поверхностного натяжения раствора ПАВ. [10] |
Поверхностное натяжение водных растворов ПАВ уменьшается с ростом концентрации вплоть до ККМ. Изотерма ст / ( 1псПАВ ( рис. 39) в области низких концентраций ПАВ имеет криволинейный участок, на котором в соответствии с уравнением Гиббса адсорбция Г на межфазной границе возрастает с ростом концентрации. В этой области на межфазной границе формируется насыщенный мономолекулярный адсорбционный слой. При дальнейшем увеличении концентрации ПАВ ( спдв - ККМ) в объеме раствора образуются мицеллы и поверхностное натяжение практически не изменяется. [11]
Поверхностное натяжение водных растворов ПАВ резко уменьшается с ростом концентрации вплоть до ККМ, а затем остается постоянным. Преимущество этого метода определения ККМ заключается в том, что точность определения положения точки перегиба ( и, следовательно, ККМ) почти одинакова для веществ с длинной и короткой цепями, так как поверхностное натяжение изменяется во всех случаях практически на одну и ту же величину. С другой стороны, точность других методов, основанных на измерениях электропроводности, показателя преломления, осмотического давления, парциального молярного объема и др., уменьшается почти обратно пропорционально значениям ККМ. [12]
Поверхностное натяжение водных растворов перекиси водорода измерено Шпрингом [36], Маасом и Хэтчером [11] и Фиббсом и Жигером [29] методом капиллярного поднятия. Судя по сравнению с данными, полученными Шпрингом для воды, его данные для растворов перекиси, по-видимому, отличаются значительной погрешностью. Результаты измерений Фиббса и Жигера не согласуются с данными Мааса и Хэтчера. [13]
Исследуя поверхностное натяжение водных растворов органических веществ, Траубе ( 1891) установил правило, что в любом гомологическом ряду при слабых концентрациях удлинение углеродной цепи на СШ - группу увеличивает поверхностную активность в 3 - 3 5 раза. Лангмюр выяснил, что правило Траубе справедливо лишь при свободном расположении адсорбированных молекул в поверхностном слое параллельно поверхности, что также соответствует их газовому состоянию. [14]
Исследуя поверхностное натяжение водных растворов органических веществ, Траубе ( 1891) установил правило, что в любом гомологическом ряду при слабых концентрациях удлинение углеродной цепи на СН2 - группу увеличивает поверхностную активность в 3 - 3 5 раза. Лэнгмюр выяснил, что правило Траубе справедливо лишь при свободном расположении адсорбированных молекул в поверхностном слое параллельно поверхности, что также соответствует их газовому состоянию. [15]
Страницы: 1 2 3 4