Поверхностное натяжение - водный раствор
Cтраница 3
На рис. 2 представлены кривые зависимости поверхностного натяжения водных растворов исследуемых эмульгаторов и их смеси ( весовое соотношение 1: 1) при 20 С от концентрации. На основании этих кривых были расчитаны и построены изотермы адсорбции Гиббса для каждого индивидуального вещества и их смеси. [31]
На рис. 2 представлены кривые зависимости поверхностного натяжения водных растворов исследуемых эмульгаторов и их смеси ( весовое соотношение 1: 1) при 20 С от концентрации. На основании этих кривых были засчитаны и построены изотермы адсорбции Гиббса для каждого индивидуального вещества и х смеси. [33]
Наиболее важными свойствами моющих веществ являются: поверхностное натяжение водных растворов на границе с воздухом и с другой фазой, моющее действие, пенообразование, способность диспергировать кальциевые мыла, суспендирующие свойства, защитное действие. [34]
 |
Зависимость удельной электропроводности от концентрации ионного ПАВ.| Графическое определение мицеллярнои массы ПАВ по мутности. [35] |
Другой метод определения ККМ основан на измерении поверхностного натяжения водных растворов ПАВ, которое резко уменьшается с ростом концентрации ( см. рис. VI. [36]
Подробные исследования поверхностной активности, кинетики установления равновесного поверхностного натяжения водных растворов, вязкости поверхностных слоев и двусторонних пленок, устойчивости пленок и пен в таких растворах и смесях с другими ПАВ не проводились. Изучению этих свойств и посвящена данная работа. [37]
Критерием чистота служило отсутствие минимума на изотерме поверхностного натяжения водного раствора ДСН. [38]
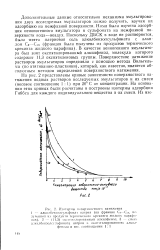
Поскольку в литературе отсутствуют данные об изменении поверхностного натяжения водных растворов смоляных и жирных кислот, а также щелочного лигнина от их концентрации, нами были проведены такие исследования. Лигнин и суммарно смоляные и жирные кислоты были выделены из сточных вод и приготовлены водные растворы щелочного лигнина и натриевых солей кислот различной концентрации. Поверхностное натяжение разбавленных водных растворов щелочного лигнина и натриевых солей смоляных и жирных кислот ( суммарно) определено методом максимального давления пузырька воздуха в приборе П. А. Ребиндера при 20 С. Как видно из приведенных данных ( рис. 1), поверхностное натяжение водных растворов солей смоляных и жирных кислот с повышением их концентрации до 4 8 г / л ( критическая концентрация мицеллообразования - ККМ) резко падает. Дальнейшее повышение концентрации мыл не оказывает влияния на поверхностное натяжение растворов. В сульфатном мыле смоляные и жирные кислоты содержатся в соотношении 1: 1 с небольшим отклонением в ту или другую сторону. Из жирных кислот главным образом содержится пальмитиновая кислота и в небольшом количестве олеиновая и лино-левая кислоты. Для всех этих кислот характерно линейное строение их молекул, причем длина их значительно превышает поперечные размеры. Смоляные кислоты представляют собой смесь, по составу близкую к абиетиновой кислоте. Все они имеют кольчатое строение, причем длина и поперечник молекул имеют одинаковые размеры. Имея различное строение, смоляные и жирные кислоты обладают и различными поверхностно-активными свойствами. Поверхностные свойства у смоляных кислот выражены несколько слабее, чем у жирных. Этим и следует объяснить, что ККМ смеси кислот достаточно высока. [39]
 |
Значения постоянной q, применяемой для оценки межфазного натяжения. [40] |
Вследствие того что вода является полярным веществом, оценка поверхностного натяжения водных растворов представляет собой особую задачу. Можно выделить три фазы - пар, жидкость и еще одну фазу, которую представляет собой межфазная область, в ряде случаев сильно отличающуюся по своим свойствам от однородной жидкости. [41]
В УфНИИ разработан специальный прибор - сталагмометр для измерения поверхностного натяжения указанных водных растворов, позволяя тем самым контролировать концентрацию ПАВ. [42]
Для контроля продукт проверяют по величине рН раствора, поверхностному натяжению водного раствора, содержанию влаги. [43]
Он показал, что концентрация, необходимая для одинакового понижения поверхностного натяжения водных растворов в любом гомологическом ряду, уменьшается на каждую дополнительную группу СН2 приблизительно в три раза. Лангмюр показал, что эта закономерность соответствует возрастанию работы адсорбции с введением в молекулу групп СН2 в арифметической прогрессии. [44]
В сравнении с ионными ПАВ ПЭГ обладают сравнительно низкой поверхностной активностью: поверхностное натяжение водных растворов почти в 2 раза выше, чем у ионных ПАВ. [45]
Страницы: 1 2 3 4