Начало - отсчет - энтальпии
Cтраница 1
Начало отсчета энтальпии i не имеет принципиального значения, наиболее применительно значение i 0 при О С. [1]
За начало отсчета энтальпии для газов может быть принята температура Т 0 К. [2]
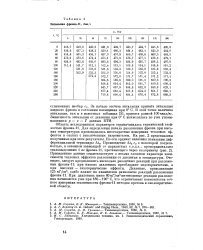 |
Энтальпия фреона-11, дж / г. [3] |
За начало отсчета энтальпии принята энтальпия жидкого фреона в состоянии насыщения при 0 С. В этой точке величина энтальпии, как и в известных таблицах [5], принята равной 100ккал / кз. [4]
Произвольный выбор начала отсчета энтальпии для отдельных компонентов может привести к тому, что при некоторой температуре значение энтальпии парового потока, богатого легкими компонентами, будет близким к значению энтальпии жидкостного потока, богатого тяжелыми компонентами. Следовательно, в процессе приближения знаменатель уравнения ( 111 33) может иметь значение, близкое к нулю, и результат расчета будет далеким от истинного. [5]
Константа интегрирования определяет начало отсчета энтальпии, поэтому несущественна. Мы полагаем ее для простоты равной нулю. [6]
Предположим, что начало отсчета энтальпии воздуха в газовой фазе принято при температуре 273 15 К. [7]
Таким образом, за начало отсчета энтальпии и энтропии воды условно принимаем точку на кривой жидкости, где t 0 С и р0 0 00623 ата. Полагаем, что в рассматриваемых условиях ( / о 0 и s0 0) допустимо считать начальное значение внутренней энергии также равным нулю. [8]
При этом получается обычно принимаемое начало отсчета энтальпии и энтропии. [9]
 |
Изотермы реального газа в р, и-диаграмме.| Зависимость теплоты парообразования воды от ее температуры. [10] |
Для различных веществ точка начала отсчета энтальпии ( или внутренней энергии) выбирается произвольно. Для воды за начало отсчета внутренней энергии принимается тройная точка воды ( р 0 611657 кПа, t 0 01 С); энтальпия воды в тройной точке близка к нулю и составляет 0 00061 кДж / кг. [11]
 |
Энтальпия воды при температуре 100 С. [12] |
Для различных веществ точка начала отсчета энтальпии ( или внутренней энергии) выбирается произвольно. [13]
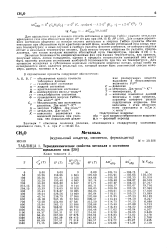 |
Термодинамические свойства метаналя в состоянии идеального газа. [14] |
Для конденсированного состояния вещества за начало отсчета энтальпии и энергии Гиббса приняты обычно энтальпия при абсолютном нуле кристаллической фазы, наиболее устойчивой при самых низких температурах; в иных случаях в скобках указаны фазовое состояние, от которого ведется отсчет и начальная температура отсчета. [15]
Страницы: 1 2 3 4