Начало - отсчет - энтальпии
Cтраница 3
Часто начало отсчета энтальпии выбирают таким образом, чтобы при некоторой базисной температуре энтальпии химических элементов равнялись нулю. Тогда энтальпия соединения при базисной температуре будет равна изменению энтальпии за счет реакции образования соединения из реагирующих компонентов, или так называемой теплоте образования соединения. [31]
При различных тепловых расчетах в технике и при анализе циклов энергетических установок ( см. § 5 - 9) интересуются не абсолютными значениями энтальпий, а их изменениями в соответствующих процессах, поэтому нулевое значение энтальпии в этих случаях выбирают условно при каких-либо значениях температуры и давления. Строго говоря, начало отсчета энтальпии связано с началом отсчета внутренней энергии. В соответствии с международным соглашением для воды за нулевое значение принимается значение внутренней энергии при температуре 273, 16 К. [32]
Очевидно, что метод линеаризации можно применить к задачам, для которых число Люиса газовой фазы не равно единице. Необходимо только еще раз выбрать начало отсчета энтальпии описанным выше способом. Здесь этот случай не обсуждается. [34]
При создании таблиц полных энтальпий за начало отсчета энтальпии элементов било принято их стандартное состояние, нанбо тее распространенное в природе ( О. [35]
Крайняя нижняя изобара р ртр своим прямолинейным участком разграничивает области равновесных двухфазных состояний насыщенный пар - жидкость и твердое тело - насыщенный пар. В случае, когда за точку начала отсчета энтальпии и энтропии принимают состояние тройной точки ( как, например, для Н2О), эта изобара проходит через начало координат. [36]
Нижняя изобара р - ртр своим прямолинейным участком разграничивает области равновесных двухфазных состояний жидкость-газ и твердое тело-газ. В случае, когда за точку начала отсчета энтальпии и энтропии принимают тройную точку ( как, например, для воды), эта изобара проходит через начало координат. [37]
Это верно лишь при условии химической инертности компонента в рассматриваемом процессе. При наличии в системе химических реакций начала отсчета энтальпии компонентов, участвующих в реакции, нельзя выбирать совершенно произвольно. [38]
В первом томе учтены изменения в термодинамических константах веществ по данным справочника [62] и соответственно исправлены нулевые члены полиномов AIt АЗ. В данном томе используется система с началом отсчета энтальпии при 298 15 К. [39]
При обсуждении в § 6 - 5 формулы Меркеля для теплового потока / - - поверхности уже отмечалось, что соответствующий выбор начала отсчета энтальпии позволяет выразить q L через одно свойство газовой фазы - энтальпию. Далее, почти горизонтальное расположение изотермы смешанной фазы на рис. 7 - 30 указывает на целесообразность выбора для смеси Н2О - воздух общепринятого начала отсчета энтальпии. При этом и для жидкости, и для газа нужно принимать значения параметров состояния такие же, как в рассматриваемой градирне. [40]
В таблице для ксенона за начало отсчета энтальпии принят О К, а в таблице для гелия О С. Поэтому при подсчете энтальпии смеси следует к значению / не прибавить значение i 0 1428 3 кДж / кг, указанное в начале таблицы термодинамических свойств гелия, чтобы начало отсчета энтальпии компонентов было общим. [41]
 |
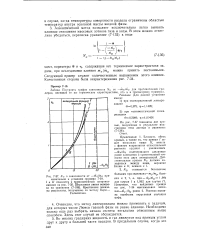
Энтальпия углеводородов ЛЯ ( в жидкой фазе, отсчитанная от температуры плавления, при температуре кипения в зависимости от числа атомов углерода п в молекуле. [42] |
Она сводится к графическому нахождению энтальпии при заданной температуре по известным значениям плотности топлива при температуре 20 С и величины: характеристического фактора. Погрешность определения энтальпии жидкости составляет в среднем 3 %, паров 12 кДж / кг. За начало отсчета энтальпии пара и жидкости в данной методике приняты ее значения при температуре минус 129 С. [43]
Следует подчеркнуть, что абсолютное значение энтальпии ( так же как и абсолютное значение внутренней энергии) не может быть ни измерено, ни вычислено термодинамическими методами; эксперимент и термодинамический расчет позволяют определить лишь изменение энтальпии или внутренней энергии вещества. Именно эта разность и представляет интерес для теплотехнических расчетов. Для расчета изменения энтальпии безразлично, какое состояние вещества выбрано за начало отсчета энтальпии. [44]
Выражение ( 4) в общем случае отлично от 0 и по абсолютной величине равно температурному изменению теплового эффекта химической реакции при постоянном давлении в пределах рассматриваемых температур. Очевидно, чем больше температурная зависимость теплового эффекта, тем больше отличаются значения сравниваемых величин. Таким образом, согласно ( I) тепловая мощность трубчатого реактора зависит от выбора температуры начала отсчета энтальпии и, следовательно, ье является величиной объективной, обусловленной параметрами процесса. [45]
Страницы: 1 2 3 4