Данный белок
Cтраница 1
Иногда данный белок принимает то одну, то другую конформацию. [1]
Как данный белок, так и продукты его расщепления могут выполнять физиологические функции; специфический протеолиз все эти функции подавляет. [2]
Связываемость данного белка увеличивается до определенного предела с удлинением гидрофобной ножки; это показано десорбцией белка с колонки, для которой необходимы жесткие условия. [3]
Характерное для данного белка двумерное расположение пептидов, образующихся при его частичном гидролизе. [4]
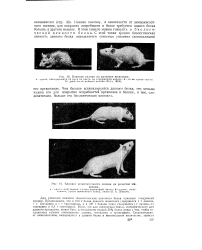 |
Влияние валина на развитие животных.| Влияние недостаточности лизина на развитие животных. [5] |
Чем больше ассимилируется данного белка, тем меньше нужно его для покрытия потребностей организма в белках, и тем, следовательно, больше его биологическая ценность. [6]
При гидролизе каждого данного белка могут образоваться все эти - аминокислоты или только некоторые из них в разных пропорциях для каждого белка. Из 20 различных аминокислот можно построить 2 3 - 1018 изомеров белковой молекулы, что подчеркивает сложность определения структуры и осуществления синтеза белков. [7]
Этот метод позволяет определять концентрацию данного белка в белково смеси при условии, что исследователь располагает соответствующей моноспецифической антисывороткой. В качестве примера ниже описана методика определения концентрации IgG в сыворотке крови. [8]
РНК и затем переводится в специфичную для данного белка последовательность аминокислот. [9]
Биологическую питательную ценность белков определяют сравнением всех свойств данного белка и прежде всего его аминокислотного состава с наиболее ценными и хорошо усвояемыми белками куриного яйца. [10]
Биологическую питательную ценность белков определяют сравнением всех свойств данного белка и прежде всего его аминокислотного состава с наиболее ценными и хорошо усвояемыми белками куриного яйца. [11]
Клонированная описанным выше способом кДНК не идентична природному гену данного белка, поскольку она не содержит нитронов, которые обычно присутствуют во многих ( если не в большинстве) эукариотических генах, кодирующих белки ( разд. Вспомним, что после коллинеарного матричного синтеза мРНК на таких генах в ходе обычной биологической транскрипции участки мРНК, комплементарные интронам в ДНК, вырезаются до трансляции мРНК на рибосомах ( разд. [12]
Первый вопрос, который возникает: каков суммарный аминокислотный состав данного белка. Фишера ушла далеко вперед по точности ( достигающей 99 %) и по скорости операции. [13]
Первый вопрос, который возникает: каков суммарный аминокислотный состав данного белка. Фишера ушла далеко вперед по точности ( достигающей 99 %) и по скорости операции. Аминокислоты вымываются в порядке уменьшающейся кислотности; под конец, при буфере рН 11, идет вымывание диаминокислот. [14]
Последовательность аминокислот в первичной структуре белка является специфической видовой характеристикой данного белка. [15]
Страницы: 1 2 3 4