Данный белок
Cтраница 2
Электростатические взаимодействия играют существенную роль только вдали от изоэлектрической точки данного белка; заряженные звенья располагаются только на поверхности глобулы. [16]
После того как был выяснен аминокислотный состав и установлен молекулярный вес данного белка, необходимо было определить, в какой последовательности соединяются аминокислоты в его молекуле. Для того чтобы представить всю трудность этой задачи, допустим, что данный белок построен только из 1 1 различных аминокислот и что каждая аминокислота встречается в молекуле только один раз. Другими словами, из 11 различных аминокислот, встречающихся в молекуле только один раз, теоретически можно построить 40 000 000 изомеров. Синтезировать такое количество изомеров и сравнить их свойства с исследуемым белком совершенно невозможно. Если мы снимем вышеуказанные ограничения и примем во внимание, что в белках нередко содержится около 20 различных аминокислот, то количество возможных изомеров белка возрастет до астрономических величин. [17]
Далее, исследование структурных формул белков показало, что все молекулы данного белка математически тождественны друг другу, и только в результате генетической мутации может появиться измененная мутированная клетка, способная синтезировать измененный белок, причем все молекулы этого измененного белка также идентичны друг другу. Впервые Ингрэм на примере гемоглобина, а затем многие другие ученые показали, что простая генетическая мутация приводит к изменению одного единственного аминокислотного звена в полипептидной цепи белка. При этом свойства белка могут сильно измениться, хотя химическое повреждение и кажется весьма незначительным. Это проистекает из того, что макромолекулы белков свертываются в спиральную вторичную структуру вследствие образования огромного числа внутримолекулярных водородных связей, а спиральные участки изгибаются и складываются в компактную третичную структуру, определяемую весьма тонким балансом различных молекулярных сил сцепления и отталкивания. Часто изменение природы одного звена цепи может вызвать катастрофические изменения третичной структуры. [18]
Проиллюстрируем это обстоятельство сопоставлением хроматографических этапов двух недавно опубликованных методов очистки данного белка. [19]
Здесь предполагается, что в растворе присутствуют только мономеры и димеры данного белка. [20]
В результате мы имеем синтетическую кДНК, которая кодирует аминокислотную последовательность данного белка. [21]
После того как был выяснен аминокислотный состав и установлен молекулярный вес данного белка, необходимо было определить, в какой после довательности соединяются аминокислоты в его молекуле. Для того чтобы представить всю трудность этой задачи, допустим, что данный белок построен только из И различных аминокислот и что каждая аминокислота встречается в молекуле только один раз. Другими словами, из И различных аминокислот, встречающихся в молекуле только один раз, теоретически можно построить 40 000 000 изомеров. Синтезировать такое количество изомеров и сравнить их свойства с исследуемым белком совершенно невозможно. Если мы снимем вышеуказанные ограничения и примем во внимание, что в белках нередко содержится около 20 различных аминокислот, то количество возможных изомеров белка возрастет до астрономических величин. [22]
В принципе, все вышесказанное не обязательно относится к максимизации ферментативной активности данного белка в клетке. Варьирование соотношения аллелей в клетке позволяет как угодно приближаться к необходимой ферментативной активности в клетке. А эта активность может быть и минимальной, и промежуточной. Самое главное то, что этим свойством могут обладать только мультимерные белки. [23]
Число и тип дисульфидных мостиков в разных белках различны, но для каждого данного белка число и расположение этих мостиков служат специфической характеристикой. Существуют белки, в молекуле которых дисульфидные мостики вообще отсутствуют; у других имеются мостики либо между отдельными цепями, либо внутри одной и той же цепи; наконец. [24]
Стабилизация каждой данной третичной структуры осуществляется в результате специфических взаимодействий между специфическими для данного белка аминокислотными остатками, образующими специфическую для данного белка последовательность; например, определенные карбоксилатные группировки соединены водородной связью с определенными остатками тирозина, другие карбоксилатные группы взаимодействуют электростатически с гуаниди-ниевыми группировками определенных остатков аргинина, а какие-то неполярные группировки аминокислотных остатков находятся в тесном контакте вследствие вытесняющего влияния растворителя. Вообще говоря, при изменении аминокислотного состава или последовательности аминокислот в первичной структуре характер названных взаимодействий должен изменяться, а это должно привести к образованию других конформаций белка. Свертывание в определенную конформацию, присущую данной белковой молекуле, вероятно, происходит постепенно, короткими участками, в процессе синтеза белка, поскольку соединенные аминокислотные остатки каждой вновь образованной молекулы белка отделяются от матрицы ( информационной рибонуклеиновой кислоты) в строго определенной последовательности. [25]
Так, адсорбция яичного альбумина в изоточке полимолеку-лярна, что обусловлено большой склонностью данного белка к агрегации в водных растворах. [26]
 |
Перенос UDP-активированного сахара на сериновую гидроксильную.| Полипренол долихол - промежуточный липнд, участвующий в биосинтезе N-гликозндной связи гликопротеинов. [27] |
Каждая молекула гликопротеина может включать несколько идентичных олигосахаридных цепей, которые специфичны для данного белка. Однако последовательности олигосахаридов необязательно должны быть полными: один или более моносахаридов могут отсутствовать. Структура олигосахаридов определяется специфическими гликозилтрансферазами. [28]
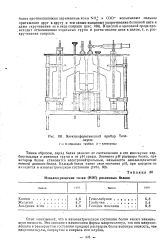 |
Электрофоретический прибор Тизе.| Изоэлектрические точки ( ИЭТ различных белков. [29] |
Значение рН раствора белка, при котором белок становится электронейтральным, называется иаоэлектрической точкой данного белка. [30]
Страницы: 1 2 3 4