Нейтрализация - слабая кислота
Cтраница 2
Кривая нейтрализации слабой кислоты сильным основанием несимметрична в отношении точки нейтрализации. [16]
Теплоты нейтрализации слабых кислот слабыми основаниями различны по своей величине и меньше, чем у сильных кислот и щелочей, так как сказываются неодинаковые значения теплот диссоциации. [17]
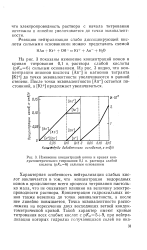 |
Изменение концентраций ионов и кривая кон. [18] |
Характерная особенность нейтрализации слабых кислот заключается в том, что концентрация водородных ионов в продолжение всего процесса титрования настолько мала, что не оказывает влияния на величину электропроводности раствора. Концентрация гидроксильных ионов также невелика до точки эквивалентности, а после нее линейно повышается. Точка эквивалентности расположена на пересечении двух восходящих ветвей кондук-тометрической кривой. [19]
Следовательно, при нейтрализации слабых кислот сильными основаниями ( и наоборот) титрование должно заканчиваться при рН не 7, а при других его значениях, соответствующих реакции раствора той соли, которая образуется в процессе титрования. Поэтому для каждого отдельного случая титрования необходимо правильно выбрать индикатор. [20]
Тепловые же эффекты нейтрализации слабых кислот сильными основаниями и сильных кислот слабыми основаниями заметно ниже. [21]
Для определения теплоты нейтрализации слабой кислоты сильным основанием собирают калориметр, как описано в работе 3 ( стр. В пробку калориметра, помимо мешалки и термометра Бекмана, вставляют ампулу для щелочи. [22]
 |
Стандартные теплоты фазовых переходов некоторых веществ. [23] |
Иная закономерность наблюдается для нейтрализации слабых кислот или ( и) слабых оснований. В этом случае теплота нейтрализации меньше, так как ионизация кислоты ( основания) требует затраты энергии. [24]
 |
Теплоты растворения некоторых веществ в воде при 25 С А иН2О ( ж - А1в лН20 ( ж 1.| Зависимость теплоты растворения H2SO4 ( ж в Н2О ( ж при 25 С от числа молей воды п. [25] |
Иная закономерность наблюдается для нейтрализации слабых кислот или ( и) слабых оснований. [26]
Величина ДЯ - теплота нейтрализации слабой кислоты сильным основанием обычно больше или меньше 57359 16 Дж / моль, так как ДЯдис может иметь положительную или отрицательную величину в зависимости от природы кислоты. [27]
Третий тип кривых характерен для нейтрализации слабых кислот. Процессы нейтрализации слабых кислот слабыми основаниями имеют следующую характерную особенность: концентрации водородных и гидроксильных ионов в продолжение всего процесса титрования настолько малы, что не могут оказывать влияния на электропроводность раствора. Изменение электропроводности раствора вызывается только увеличением концентраций анионов кислоты и катионов основания. Поэтому, чем выше подвижности этих ионов, тем сильнее увеличивается электропроводность раствора до точки эквивалентности и тем меньше угол излома. [28]
Таким образом, константа равновесия нейтрализации слабой кислоты сильным основанием определяется только отношением комстанты диссоциации слабой кислоты к ионному произведению воды. Для реакции полученное столь высокое значение кон-ста. NaCHsCOO - сильный электролит, находящийся в состоянии ионов СН3СОО - и Na; молярная концентрация ионов СН3СОО равна исходной концентрации уксусной кислоты. [29]
Определив опытным путем тепловой эффект нейтрализации слабой кислоты сильным основанием, можно на основании закона Гесса рассчитать теплоту диссоциации данной слабой кислоты. По теплоте нейтрализации, найденной в опыте, можно рассчитать количество кислоты или основания, взятое для нейтрализации. [30]
Страницы: 1 2 3