Кривая нейтрализация
Cтраница 1
Кривые нейтрализации ТТГА и ТПГА аналогичны. [1]
Кривые нейтрализации щелочноземельных элементов ( для примера на рисунке приводится титрование смеси кальция с комплексоном) практически повторяют ход кривой титрования самого комплексона, несколько спускаясь в более кислую область. Это свидетельствует о том, что комплексонаты этих элементов имеют сравнительно очень малую прочность. [2]
Форма кривой нейтрализации является функцией свойств реагирующих компонентов. Если в результате их взаимодействия состав вещества меняется, то наклон кривой в заданной точке величины рН также меняется. Возникающие при этом вторичные колебания накладываются на первичные. Такой переходный процесс не может быть рассчитан. [3]
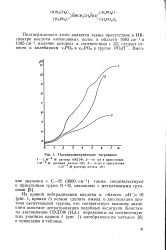 |
Потенциометрическое титрование. [4] |
Из кривой нейтрализации кислоты в области рН 10 ( рис. 1, кривая /) нельзя сделать вывод о диссоциации протона оксиэтильной группы, что соответствует высоким значениям констант депротонизации подобных оксигрупп. Константы диссоциации ОЭДТФ ( H6L) определены на соответствующих участках кривой / ( рис. 1) алгебраическим методом [6] и приведены в таблице. [5]
Отклонение полученной кривой нейтрализации соляной кислоты гидроокисью от теоретической кривой объясняется наличием химических примесей. [6]
Вычислите данные кривой нейтрализации ( см. задачу 1) и выразите результаты графически. [7]
При построении кривых нейтрализации по оси абсцисс откладывают имеющиеся в разные моменты титрования концентрации кислоты ( или щелочи), а по оси ординат - отвечающие им величины рН раствора. [8]
Различие характера отдельных кривых нейтрализации имеет большой значение для количественного химического анализа. [9]
Различие характера отдельных кривых нейтрализации имеет большое значение для количественного химического анализа. [10]
Математической обработкой кривых нейтрализации нитрило-триуксусной кислоты, полученных как при избытке кислоты, так и при избытке ионов кальция, было показано, что при образовании комплекса один моль кальция замещает один моль ионов водорода. [11]
Это соотношение представлено кривой нейтрализации, определяющей значение рН в зависимости от отношения концентрации реагента к концентрации выходящих компонентов рабочей среды. [12]
Первая буферная область кривых нейтрализации кислот ( см. рис. 54, б) является следствием диссоциации фосфоновых групп, вторая - диссоциации бетаиновых протонов. Сравнительная близость значений констант диссоциации комплексонов с гетероатомами между собой и с таковыми для пентаметилендиаминдиизопропилфосфоновой кислоты и большая разница их по сравнению с константами этиленди-аминдиизопропилфосфоновой кислоты ( см. табл. 39) свидетельствуют о том, что на константы диссоциации оказывает существенное влияние длина полиметиленового мостика между изопропилфосфоновыми группами, а не природа гетероатома. Меньшая разность между константами диссоциации бетаиновых протонов у комплексонов с гетероатомами по сравнению с соответствующими величинами производных этилендиамина объясняется уменьшением взаимного влияния бетаиновых атомов азота. [13]
На основании формы кривых нейтрализации урамилдиуксусной кислоты в присутствии различных катионов Шварценбах пришел к заключению, что образующиеся комплексные соединения содержат всегда только один анион кислоты Xs - и что при их образовании выделяется только один ион водорода. [14]
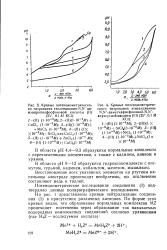 |
Кривые потенциометрическо.| Кривые потенциометриче. [15] |
Страницы: 1 2 3 4