Кривая нейтрализация
Cтраница 3
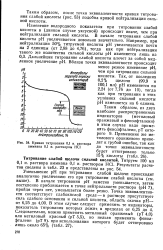 |
Кривая титрования 0 1 н. раствора дет к ГРУ6 Й ошибке, так как аммиака 0 1 н. раствором НС1 ДО точки эквивалентности. [31] |
Таким образом, после точки эквивалентности кривая титрования слабой кислоты ( рис. 53) подобна кривой нейтрализации сильной кислоты. [32]
Таким образом, после точки эквивалентности кривая титрования слабой кислоты ( см. рис. 36) подобна кривой нейтрализации сильной кислоты. [33]
Таким образом, после точки эквивалентности кривая титрова -, ния слабой кислоты ( см. рис. 49) подобна кривой нейтрализации сильной кислоты. [34]
 |
Изменение рН смесей НА и Et NA. [35] |
ДМСО намного меньше, чем в АН, кривая нейтрализации упомянутой выше формы системы в ДМСО имеет большее сходство с кривой нейтрализации в воде. [36]
Если кислота сравнительно сильно ионизирована, линия нейтрализации имеет форму кривой до точки эквивалентности, и трудно наитие достаточной степенью точности точку пересечения кривой нейтрализации с линией гидроокиси натрия. Последняя является той прямой линией, которую находят после прибавления некоторого избытка основания. [37]
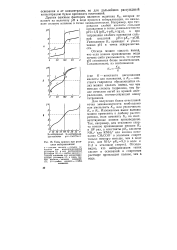 |
Типы кривых при реакциях нейтрализации. [38] |
К - константа диссоциации кислоты или основания, а Кн - константа гидролиза образующейся соли) можно сделать вывод, что чем меньше степень гидролиза, тем более отчетлив изгиб на кривой нейтрализации, соответствующий концу титрования. [39]
Шварценбах [24] рассматривает равновесия, которые могут возникать при комплексообразовании между ионами металла и полиаминами, а для общего случая приводит также подробный анализ метода определения констант образования таких комплексов из соответствующих кривых нейтрализации. Согласно приведенным данным, этот метод особенно удобен для исследования комплексов, содержащих одну молекулу полиамина на каждый центральный ион. Путем соответствующего выбора экспериментальных условий ( изменение отношения ионов металла к полиамину) число теоретически возможных равновесий можно свести к минимуму, что упрощает математическую об работку данных измерений. [40]
Грегор и Врегман [48] опубликовали кривые титрования для ряда смол известного химического состава, которые определенно показывают, что некоторые смолы содержат два или большее число типов кислотных групп, характеризующихся отчетливыми точками перегиба на кривых нейтрализации. Кривые скорости обмена при различных значениях рН показывают, что сильно кислотные группы нейтрализуются быстрее, чем слабо кислотные группы. [41]
В случае необходимости можно вывести уравнения, описывающие изменение рН в процессе нейтрализации после первой эквивалентной точки, подобные тем, которые были приведены ранее, но в большинстве случаев можно ограничиться более простым снособом описания всей кривой нейтрализации. [42]
По теории Аррениуса могут быть рассчитаны кривые нейтрализации, характеризующие изменение рН раствора при нейтрализации кислоты или основания. Рассмотрим кривые нейтрализации для буферного раствора, состоящего из слабой кислоты НА и ее соли с сильным основанием. В результате при некотором соотношении концентрации соли и кислоты рН системы при добавлении кислоты или щелочи изменяется незначительно. [43]
По теории Аррениуса могут быть рассчитаны кривые нейтрализации, характеризующие изменение рН раствора при нейтрализации кислоты или основания. Рассмотрим кривые нейтрализации для буферного раствора, состоящего из слабой кислоты НА и ее соли с сильным основанием. В результате при некотором соотношении концентрации соли и кислоты рН системы при добавлении кислоты или щелочи изменяется незначительно. [44]
На кривой нейтрализации ( рис. 1, кривая 1) можно выделить буферные области: о а 2; 2 С а 3; 3а4; 4 а 5 и 5 а 6, свидетельствующие о том, что при низких значениях рН отщепляются в одной буферной области два протона, а в дальнейшем в каждой буферной области по одному протону. [45]
Страницы: 1 2 3 4