Необратимость - электродный процесс
Cтраница 3
Для установления обратимости постояннотокового электродного процесса обычно необходимо строго доказать, что выдерживаются определенные критерии ( см. гл. Существенно, что обратимость или необратимость электродного процесса в переменнотоковой полярографии должна бы определяться даже более строго, чем в случае постояннотоковой. Временная шкала в переменнотоковой полярографии зависит в основном, хотя и не полностью, от частоты, и возможно, что электродный процесс, обратимый в постояннотоковой полярографии, будет необратимым во временной шкале переменнотоковой полярографии. [31]
Так, стабильная разнос п потенциалов между индикаторными электродами была получена только при избытке ионов двухвалентного железа. При избытке бихрома-та наблюдалась нестационарность, обусловленная необратимостью электродного процесса. [32]
Аскорбиновая кислота окисляется на платиновом электроде, и на вольт-амперной кривой имеется область предельного тока, менее отчетливо выраженная, чем в случае окисления гидрохинона. Нечеткая форма вольт-амперной кривой свидетельствует о высокой степени необратимости электродного процесса. [33]
Если приложить к электролизеру напряжение, равное напряжению разложения ( 1 23 в при 25 С), то фактически разложения воды происходить не будет. Такое значительное различие между теоретическим и экспериментальным напряжением разложения обусловлено необратимостью электродных процессов, которые с заметной скоростью протекают только при достаточной поляризации. [34]
Первое слагаемое пРл определяет количество энергии, выделяющейся в виде тепла в результате необратимости электродного процесса. [35]
Во многих случаях логарифмические графики необратимых волн почти линейны, однако их наклон не равен п, а часто соответствует переносу как будто бы не целого числа электронов. Наклон, не равный целому числу п, в общем может служить доказательством необратимости электродного процесса, однако, как будет видно из дальнейшего, это правило не всегда верно. [36]
В соответствии с уравнением (49.11) тепловой эффект отдельного электродного процесса - ДЯ состоит из двух слагаемых. Первое слагаемое nFr определяет количество энергии, выделяющейся в виде теплоты, в результате необратимости электродного процесса. [37]
Физико-механические свойства электролитических осадков являются существенной характеристикой качества покрытий и определяют их применимость в той или иной области техники. Свойства электролитических осадков обусловлены наличием включений в них разнообразных чужеродных частиц, а также степенью необратимости электродного процесса ( величиной перенапряжения) при восстановлении ионов металлов. Последнее обстоятельство связано с тем, что восстанавливающийся ион, проходя через двойной электрический слой, имеющий большую напряженность электрического поля ( порядка 107 в / см), приобретает большую скорость, которую он сразу теряет при вхождении в кристаллическую решетку; это приводит к образованию неравновесной кристаллической решетки с измененными параметрами. [38]
Коэффициент переноса а входит во многие полярографические уравнения, и он имеет большое значение в теории кинетики электродных процессов. Однако этот параметр не является константой скорости, и поэтому не помогает нам в определении обратимости или необратимости электродного процесса. Мы можем считать его просто поправочным параметром, который при использовании его вместе с константой скорости гетерогенной реакции переноса заряда облегчает полное математическое описание электродного процесса. Отметив, что а выполняет эту функцию, и записывая его во многие уравнения, мы больше не будем обсуждать этот параметр, так как для аналитических применений полярографии этого не требуется. [39]
Если исследуемый раствор содержит несколько компонентов, то на полярограмме переменного тока будет несколько максимумов, каждый из которых качественно и количественно определяет свой компонент. Полярография с использованием переменного тока может быть применена для исследования различных электрохимических процессов, таких, как обратимость и необратимость электродных процессов и емкость двойного электрического слоя, для изучения органических соединений и для определения микропримесей. Большим преимуществом ее перед классической и до некоторой степени осциллографической полярографией является большая чувствительность и разрешающая способность полярографов переменного тока. Последние могут быть использованы для непрерывного контроля технологического процесса. [40]
В последнем случае внутри области адсорбции при определенном потенциале наблюдаются экстремальные значения емкости, связанные с переориентировкой, частиц в смешанном адсорбционном слое. Показано, что в случае электрокристаллизации металлов совместное введение ряда высокомолекулярных аминов и фено-ло ( Гили нафтолов приводит, наряду с ростом степени необратимости электродных процессов, к резкому изменению качества катодных отложений олова, кадмия, меди и сплавов, которые становятся значительно более мелкокристаллическими плотными и равномерными, а в отдельных случаях зеркально-блестящими. [41]
Величина анодного тока зависит от поверхности ртутной капли, с увеличением которой увеличивается анодный ток. Наблюдается зависимость между отношением поверхности электрода, на котором происходит электродная реакция, и объемом, в котором происходит процесс ( S / V); оптимальное значение этой величины приблизительно равно 0.1. Величина анодного тока зависит также от степени необратимости электродного процесса, скорости перемешивания раствора в процессе накопления, длительности электролиза, температуры и других факторов. [42]
В самом общем виде электродный процесс состоит из стадию переноса заряда ( гетерогенная реакция), химических реакций. Кроме того, часто приходится учитывать адсорбцию HI другие поверхностные явления. Удобно поэтому рассматривать-обратимость или необратимость электродного процесса не только в общем виде, но и в рамках стадий электрохимического переноса заряда и химических реакций. Электродный процесс, протекающий на границе раздела электрод - раствор, может быть необратимым из-за замедленности либо стадии переноса электрона ( гетерогенная константа: скорости), либо химической реакции ( гомогенная константа скорости), либо адсорбции, и данный полярографический метод может отразить электродный процесс совершенно по-разному в-зависимости от причины необратимости или кинетического усложнения. Если причиной необратимости является стадия переноса электрона, то это часто диктует использование данного конкретного полярографического метода, а не другого. Если же необратимость имеет химическую природу, то возникают значительные сложности, как это будет видно из дальнейшего обсуждения. [43]
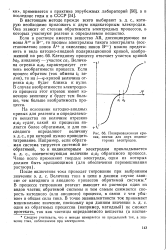 |
Поляризационная кривая, снятая для двух индикаторных электродов. [44] |
Катодному процессу отвечает участок кривой Ьа2, анодному - участок са. Величина отрезка а а2 характеризует степень необратимости процесса. Если процесс обратим ( ток обмена г о велик), то на t - ф-кривой величина отрезка а а2 будет близка к нулю. В случае необратимости электродного процесса этот отрезок имеет конечную величину и будет тем больше, чем больше необратимость процесса. [45]
Страницы: 1 2 3 4