Пятивалентный нептуний
Cтраница 1
Пятивалентный нептуний восстанавливается до четырехвалентного гидроксиламином, йодистым водородом, ионами двухвалентного железа, щавелевой кислотой в присутствии ионов Мп2 или SiFl - и электролитически. [1]
Ион пятивалентного нептуния NpO - большой ион с одним зарядом, поэтому ожидается, что он будет обладать малой способностью к комплексообразованию с любыми анионами. [2]
Ион пятивалентного нептуния NpO y -, как большой отдельно заряженный катион, с трудом комплектуется, осаждается пли экстрагируется органическими растворителями. В отличие от аналогичных ионов урана н плутония нептуний ( V) устойчив к диспропорционированию на четырех - и шестивалентное состояния, исключая сильнокислые растворы. Известны также оксалатпые комплексы в растворе. [3]
Особого внимания заслуживают твердые соединения пятивалентного нептуния. Найгон, Пеннемен, Старицкий, Кинен и Эспри [32] получили кристаллический карбонат калия и пятивалентного нептуния. Это соединение имеет ромбическую структуру, но точно состав и структура его еще не выяснены. По-видимому, единственным хорошо исследованным соединением пятивалентного нептуния является оксалат. [4]
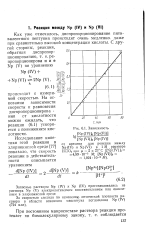 |
Зависимость [ Np ( IV ] 0 [ Np ( VI ]. [5] |
Как уже отмечалось, диспропорционирование пятивалентного нептуния происходит очень медленно, даже при сравнительно высокой концентрации кислоты. [6]
Нептуноилхлорид NpO201 образуется при растворении гидроокиси пятивалентного нептуния в соляной кислоте. [7]
Съеблум и Хайндмен 133 ] исследовали диспропорционирование пятивалентного нептуния в зависимости от концентрации хлорной кислоты; при этом для наблюдения за ходом реакции применялся спектрофотометр. [8]
Кислый оксалат нептуноила NpCbHCaC получается обработкой гидроокиси пятивалентного нептуния раствором щавелевой кислоты. [9]
Этот окисел также образуется при взаимодействии соединений четырех - и пятивалентного нептуния с NO2 при 300 - 400 С. Закись-окись нептуния легко растворяется в кислотах. Растворение NpsO8 в НС1О4 и последующие спектрофото-метрические исследования [349] показали, что в растворе присутствуют только ионы пяти - и шестивалентного нептуния. В подобных условиях растворение U3O8 приводит к образованию четырех - и шестивалентного урана. [10]
Нептуний в растворе обладает несколькими устойчивыми степенями окисления; в частности, очень устойчив пятивалентный нептуний. Химия водных растворов нептуния более сложна, чем химия водных растворов урана. Хайндмен с сотрудниками [15] достигли определенных успехов при определении свойств и поведения ионов нептуния в растворах, однако еще многое остается нерешенным. В табл. 6.5 приведены препаративные методы получения и термохимические данные для различных ионов нептуния. [11]
В работе Мефодьевой [114] электрофорез на бумаге был использован для определения знака заряда комплексных ионов четырех-и пятивалентного нептуния в растворах этилендиаминтетрауксус-ной кислоты. [12]
ЗОЛОТОЕ [20] исследовали экстракцию 1-нитрозо - 2-нафтолата уранила, они же совместно с Е. С. Пальшиным [21, 22] - экстракцию 1-нитрозо - 2-нафтолата пятивалентного нептуния. В последних двух работах вообще впервые была установлена возможность экстракции пятивалентных актинидов. [13]
Трехвалентный плутоний взаимодействует с арсеназо III примерно при тех же условиях, при которых протекают соответствующие цветные реакции редкоземельных элементов, пятивалентный нептуний - в нейтральных средах, а пятивалентный протактиний - в сильнокислых средах. Для реакций Np ( V) и Ра ( V) с арсеназо III нет соответствующих аналогий среди реакций арсеназо III с другими элементами. [14]
Наиболее прочным из окислов нептуния является двуокись NpO2, получаемая при прокаливании гидроокиси Np ( OH) 4 п Н2О или нитратов четырех - и пятивалентного нептуния. [15]
Страницы: 1 2 3