Термодинамическая неустойчивость
Cтраница 3
Окислительное действие озона обусловливается термодинамической неустойчивостью его молекул. [31]
Причиной коррозии металлов является их термодинамическая неустойчивость в коррозионной среде. [32]
Особенностью коллоидных систем является их термодинамическая неустойчивость, которая является следствием значительного избытка свободной энергии на сравнительно большой границе поверхности раздела фаз. Такой процесс называется коагуляцией коллоидных частиц и в определенных условиях он может протекать самопроизвольно. [33]
Особенностью коллоидных систем является их термодинамическая неустойчивость, которая является следствием значительного избытка свободной энергии на сравнительно большой границе поверхности раздела фаз. [34]
При больших степенях переохлаждения возрастает термодинамическая неустойчивость аустенита, а скорость диффузии углерода резко падает. При переохлаждении аустенита в эвтектоидной стали до 240 С подвижность атомов углерода близка к нулю и происходит бездиффузионное превращение аустенита. При этом меняется лишь тип решетки у - а, а весь углерод, ранее растворенный в решетке аустенита, остается в решетке феррита, хотя равновесна я концентрация углерода в феррите не превышает 0 006 % при комнатной температуре. [35]
Выше мы видели, что термодинамическая неустойчивость дисперсных и коллоидных систем выражается в самопроизвольном укрупнении частиц - коагуляции или коалесценции. Однако скорость коагуляции может быть различной. S поверхности раздела фаз достаточно велики, то коагуляция идет с большой скоростью. Такие системы называют агрегативно неустойчивыми. Но иногда в коллоиде с такой же степенью дисперсности коагуляция идет очень медленно, практически незаметно. В таких системах, называемых агрегативно устойчивыми, очевидно, поверхностное натяжение на границе фаз невелико. [36]
Выше мы видели, что термодинамическая неустойчивость дисперсных и коллоидных систем выражается в самопроизвольном укрупнении частиц - коагуляции и коалесценции. Однако скорость коагуляции может быть различной. S поверхности раздела фаз достаточно велики, то коагуляция идет с большой скоростью. Такие системы называют агрегативно неустойчивыми. Но иногда в колЛоиде с такой же степенью дисперсности коагуляция идет очень медленно, практически незаметно. В таких системах, называемых агрегативно устойчивыми, очевидно, поверхностное натяжение на границе фаз невелико. [37]
Почему же, несмотря на термодинамическую неустойчивость ( AF0), нефтяные эмульсии ( как и многие другие лиофобные коллоидные системы) оказываются устойчивыми кинетически, не изменяясь заметно в течение длительного времени. [38]
Причиной электрохимической коррозии металлов является их термодинамическая неустойчивость - самопроизвольное растворение при взаимодействии с электролитами, образование двойного электрического слоя на границе раздела фаз и переход металла в устойчивое окисленное состояние. [39]
До некоторой степени родственным процессом является термодинамическая неустойчивость. Если в ранней Вселенной смесь вещества и излучения прошла через что-либо типа критической точки, то термодинамические флуктуации плотности могли быть значительными и, поддерживаемые гравитацией, могли ускорить развитие структур: В модели горячей Вселенной наиболее перспективным в этом отношении периодом, по-видимому, является эпоха рекомбинации. Там, где плотность вещества выше средней плотности, плазма превращается в водород быстрее, уменьшая тем самым молекулярную массу и, следовательно, давление вещества, которое затем стремится увеличить плотность неоднородности. Можно было бы предположить, что при очень большом красном смещении существовала более сильная термодинамическая неустойчивость, но при большом Z число бар ионов в пределах горизонта относительно невелико, так что влияние неустойчивости на флуктуации в масштабе галактики было бы пренебрежимо мало. [40]
Причиной химической коррозии металлов является их термодинамическая неустойчивость в различных средах. Термодинамически стабильными в условиях на поверхности и в верхних слоях земной коры для большинства металлических элементов являются окисленные состояния - оксиды, сульфиды и другие соединения. Только оксиды золота и серебра ( Аи2Оз, AgO, Ag20s) термодинамически нестабильны в стандартных условиях. [41]
Основной причиной коррозии металлов является их термодинамическая неустойчивость в обычных условиях. Знак А свидетельствует о том, что от значения величины G в конечном ( окисленном) состоянии отнимается значение ее в начальном состоянии. Если при протекании химической или электрохимической реакции термодинамический потенциал возрастает ( AG0), то самопроизвольный процесс невозможен, а если убывает ( AG0), то самопроизвольный процесс возможен. [42]
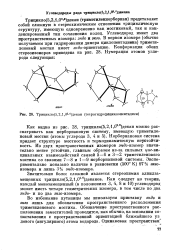 |
Трицикло ( 5 2 1 02 6 декан ( тетрагидродициклопентадиен. [43] |
Норборнановая система придает структуре жесткость и термодинамическую неустойчивость. Из двух пространственных изомеров энЗо - изомер значительно менее устойчив, главным образом из-за сильных цис-ък-цинальных взаимодействий связей 5 - 6 и 3 - 2 триметиленового мостика со связями 7 - 8 и 1 - 9 норборнановой системы. Экспериментально показано наличие в равновесии ( 500 К) 97 % экзо-изомера и лишь 3 % экдо-изомера. [44]
Другим Фактором, вызывающим коррозию, является термодинамическая неустойчивость продуктов твердения вяжущих при температуре выше 100 С. В процессе твердения традиционно применяемых вяжущих при повышенных температурах ( выше ЮО С) ускоряются как процессы собирательной рекристаллизации, так и перекристаллизации кристаллогидратов цементного камня, обуславливающие термическую коррозию цементного камня в условиях глубоких скважин. [45]
Страницы: 1 2 3 4