Двойной нитрат
Cтраница 3
После разбавления раствора водой во избежание выпадения в осадок двойных нитратов РЗЭ с обычно присутствующим в растворе Са производится экстракционное извлечение РЗЭ трибутилфосфатом. [31]
Упомянутые выше двойные соли типа квасцов и другие, а также двойные нитраты, образуемые галлием, индием и таллием с соответствующими солям и щелочных металлов, по существу тоже являются комплексными соединениями, но весьма мало устойчивы. [32]
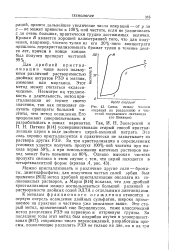 |
Связь межщу числом операций по разделению и чистотой полуяаемого лантанида ( по Вик кери. [33] |
Для дробной кристаллизации чаще всего пользу - - ются различной растворимостью двойных нитратов РЗЭ и магния, § аммония или марганца. Этот - метод может считаться классическим. [34]
Актиний и лантан отделяют от празеодима, неодима и самария дробной кристаллизацией двойных нитратов этих элементов с нитратом аммония. [35]
Наконец, метод, использованный Вельсбахом, был еще в 1871 г. предложен Менделеевым, который использовал двойные нитраты аммония для отделения лантана от дидима. Бесспорно, химическая идентификация новых элементов - старший козырь в решении проблемы дидима, но так же бесспорно, что Вельсбах не имел права игнорировать другие работы, посвященные этой важнейшей проблеме. [36]
Впоследствии было найдено, что двойные нитраты лантаноидов с магнием, а также с никелем и кобальтом пригодны для отделения европия от других элементов цериевой группы, а двойные нитраты тех же металлов с висмутом ( изоморфным с лантаноидами), по предложению Урбэна [14], были использованы для разделения двух основных групп элементов редких земель: цериевой и иттриевой. [37]
К первому типу относится обширный ряд двойных солей, многие из которых нашли применение при разделении редкоземельных элементов классическим методом дробной кристаллизации, использованным еще Д. И. Менделеевым в 1873 г. Из двойных солей редкоземельных элементов группы церия в практике дробной кристаллизации нашли применение двойные нитраты и сульфаты. Метод кристаллизации двойных сульфатов особенно пригоден для разделения редкоземельных элементов на группы церия и иттрия. [38]
Основной двойной нитрат 2Ca ( OH) 2 - Al ( OH) 2NO3 - 2H2O имеет, как и аналогичный по составу хлорид, двойную слоистую структуру. Все они в принципе имеют однотипное строение: между главными слоями, построенными из ионов Са2 с расстоянием между ними 3 32 А, располагаются промежуточные слои, расстояние которых от главного слоя зависит от величины аниона. В промежутке между слоями находится вода, связанная в большей или меньшей степени цеолитно. В большинстве случаев некоторая часть кислотных ионов может быть замещена ионами гидроксила. Это приводит к тому, что состав соединений может изменяться в определенных пределах. [39]
Основной двойной нитрат 2Са ( ОН) 3 - A1 ( OH) 2NO3 - 2H2O имеет, как и аналогичный по составу хлорид, двойную слоистую структуру. Все они в принципе имеют однотипное строение: между главными слоями, построенными из ионов Са2 с расстоянием между ними 3 32 А, располагаются промежуточные слои, расстояние которых от главного слоя зависит от величины аниона. В промежутке между слоями находится вода, связанная в большей или меньшей степени цеолитно. В большинстве случаев некоторая часть кислотных ионов может быть замещена ионами гидроксила. Это приводит к тому, что состав соединений может изменяться в определенных пределах. [40]
Подобно сульфатам, нитраты РЗЭ также легко образуют двойные соли. Марганцевые двойные нитраты значительно более растворимы, чем магниевые, причем растворимость их в воде медленно возрастает с увеличением температуры. Растворимость в азотной кислоте незначительна, и это позволяет проводить дробные кристаллизации лантанидов, пользуясь 50 % - ной азотной кислотой, так как с увеличением порядкового номера лантанида увеличивается растворимость его двойного нитрата в азотной кислоте. [41]
Основной двойной нитрат 2Ca ( OH) 2 - Al ( OH) 2N03 - 2H2O имеет, как и аналогичный по составу хлорид, двойную слоистую структуру. Все они в принципе имеют однотипное строение: между главными слоями, построенными из ионов Са2 с расстоянием между ними 3 32 А, располагаются промежуточные слои, расстояние которых от главного слоя зависит от величины аниона. В промежутке между слоями находится вода, связанная в большей или меньшей степени цеолитпо. В большинстве случаев некоторая часть кислотных ионов может быть замещена ионами гидроксила. Это приводит к тому, что состав соединений может изменяться в определенных пределах. [42]
Суммарная растворимость и природа образующегося осадка имеют такое же значение в практике разделения, как и изменение растворимости при переходе от одного элемента к следующему. Двойной нитрат магния применяется в особенности при разделении цериевой группы; бромат и диметилфосфат применяются при разделении иттриевой группы. Интересно отметить, что диметилфосфаты являются единственными известными солями редкоземельных элементов, у которых растворимость равномерно понижается от лантана до лютеция. [43]
Незначительная растворимость двойного нитрата лантана с аммонием в насыщенном растворе аммония используется в технологии получения чистого лантана. Растворимость двойных нитратов типа 2Ьп ( ЫО3) з 3Mg ( NO3) 2 - 24H2O в концентрированной азотной кислоте увеличивается от лантана к гадолинию. [44]
Результаты Эфрайма и Мезенера, измеривших спектры отражения ряда галогенидов уранила ( UO2Br2 - 7H2O, UO2F2 - 3KF, иО2Вг2 - 2КВг - 2НгО и UO2Br2 - 2NH4Br) при температуре жидкого воздуха, хорошо согласуются с этим правилом. Было показано, что спектры двойных нитратов нельзя сравнивать между собой в связи с разными кристаллическими структурами и вследствие этого различными спектрами. Подобное же смещение наблюдается в спектрах двойных галогенидов. [45]
Страницы: 1 2 3 4