Нитрит - щелочной металл
Cтраница 3
Обычно применяемый метод диазотирования состоит в обработке амина, растворенного в водной минеральной кислоте, нитритами щелочных металлов при низких температурах. [31]
К нелетучим ингибиторам относятся все уже описанные ингибиторы для нейтральных водных растворов, в первую очередь нитриты щелочных металлов, а также органические ингибиторы, добавляемые в смазки и масла. [32]
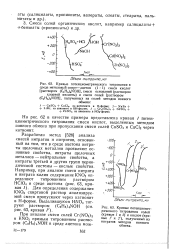
Разработан метод [528] анализа смесей нитратов и нитритов, основанный на том, что в среде ацетона нитриты щелочных металлов проявляют основные свойства, нитраты щелочных металлов - нейтральные свойства, а нитраты третьей и других групп периодической системы - кислые свойства. [34]
Разработан метод [528] анализа смесей нитратов и нитритов, основанный на том, что в среде ацетона нитриты щелочных металлов проявляют основные свойства, нитраты щелочных металлов - нейтральные свойства, а нитраты третьей и других групп периодической системы - кислые свойства. Для определения содержания KN03 спиртовой раствор анализируемой смеси пропускают через катионит в Н - форме. [36]
Ее можно использовать также для обнаружения циклогексиламина, так как это основание легко превращается в циклогексанол при нагревании с нитритом щелочного металла и соляной кислотой. [37]
Однако некоторые вещества взаимодействуют с NaN02 с образованием других продуктов реакции, таких, как N2J N20, NOj и др. у Нитриты щелочных металлов в зависимости от условий проявляют окислительные или восстановительные свойства. Примеры титриме-трических определений, основанных на таких реакциях, приведены ниже. [38]
Заслуживает внимания, что ряд соединений дает синее окрашивание даже при комнатной температуре, если их обработать концентрированной серной кислотой и прибавить нитрит щелочного металла. [39]
Однако некоторые вещества взаимодействуют с NaN02 с образованием других продуктов реакции, таких, как N2) N20, NOj и др. у Нитриты щелочных металлов в зависимости от условий проявляют окислительные или восстановительные свойства. Примеры титриме-трических определений, основанных на таких реакциях, приведены ниже. [40]
Для усиления сцепления грунтов с металлом в состав шихты часто вводят 0 5 - 2 % окислов марганца, а также нитраты и нитриты щелочных металлов. Эти вещества способствуют окислению поверхности стали под слоем грунта во время обжига покрытия, значительно улучшая прочность сцепления [ 3, стр. Предложено использовать в качестве активатора сцепления железный кек [170], основными составляющими которого являются окислы железа, меди, кобальта, никеля, натрия и кремния. Соединения серы и окись хрома, содержащиеся в железном кеке, понижают поверхностное натяжение и улучшают смачивающую способность грунта. Введение железного кека в шихту грунта позволяет полностью исключить из ее состава добавку окислов кобальта и никеля без снижения прочности сцепления грунтового покрытия с металлом. [41]
Патент США, № 4116701, 1978 г. Ингибирующая композиция в виде водного раствора, содержащая, части ( по массе): нитрита щелочного металла 5 - 12, бензоата аммония 2 - 6; алкилалканоламина 4 - 10 и азотсодержащей основы 4 - 10, используется для защиты стали в виде паров ( тумана) в процессе ее хранения и перевозки в грузовых контейнерах и вагонах. [42]
Если исследование на присутствие моно - и Диалкиланилинов проводится в присутствии анилина, последний переводят в фенол нагреванием с азотистой кислотой, точнее нитритом щелочного металла и соляной кислотой. Затем раствор подщелачивают и экстрагируют эфиром, после чего можно исследовать эфирный раствор на присутствие алкилированных анилинов. [43]
Реакцию с нитритом натрия обычно проводят в таких растворителях, как диметилформамид и диметилсульфоксид, поскольку скорость реакции в них высокая и растворимости алкилгалогенида и нитрита щелочного металла достаточны для протекания реакции. [44]
Нитриты устойчивее HN02 ( в молекуле кислоты ничтожно малый ион Н, внедряясь в электронную оболочку атома О, ослабляет связь N-О), но только нитриты щелочных металлов плавятся без разложения. При термическом разложении нитритов образуется оксид металла. Нитриты, так же как и HNO2, обладают окислительной и восстановительной активностью. В растворах они постепенно окисляются, переходя в нитраты. [45]
Страницы: 1 2 3 4