Нитробензоилхлорид
Cтраница 1
Нитробензоилхлорид был выбран в качестве этерифицирую-щего агента благодаря его доступности, высокой реакционной способности, а также большей длине волны максимума поглощения алкил-я-нитробензоатов ( 253 нм); при длине волны максимума поглощения этил-3 5-динитробензоата могут оказывать влияние примеси, поглощающие в ультрафиолетовой области. [1]
Нитробензоилхлорид чешуированный - пластинки ( чешуйки) от желтого до светло-коричневого цвета. Применяют как полупродукт в производстве азокрасителей и других продуктов. [2]
Ацилирование n - нитробензоилхлоридом позволяет в дальней-лем восстановить нитрогруппу и либо повторить реакцию ацили-зования полученного аминосоединения, либо использовать его для интеза азокрасителей. [3]
При бензоилировании n - нитробензоилхлоридом получаются продукты, содержащие нитрогруппу. [4]
Гидроксилы, реагирующие с нитробензоилхлоридом, должны быть по соседству, так как диметиласкорбиновая кислота способна реагировать с ацетоном с образованием ацетонового соединения. Оба соединения не обнаруживают наличия ни карбонильного кислорода, ни гидроксильной группы. [5]
Растворяют 1 г n - нитробензоилхлорида в 25 мл пиридина, очищенного перегонкой. Ежедневно следует приготавливать свежий раствор. [6]
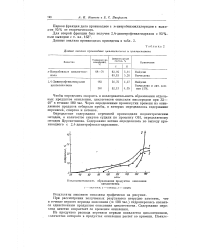 |
Данные анализа производных циклогексепола. и циклогексенона. [7] |
Первая фракция дала производное с n - нитробензоилхлоридом с выходом 95 % от теоретического. [8]
Конденсацию L-глутами новой кислоты с n - нитробензоилхлоридом проводят в воднобензольной среде с прибавлением для нейтрализации Mg ( OH) 2, Са ( ОН) 2 [184] или едкого натра [183, 185-187]; применяются и другие органические растворители, например хлороформ. [9]
Затем в воронку добавляют 1 мл раствора n - нитробензоилхлорида и встряхивают, чтобы перемешать содержимое. Оставляют смесь на 30 мин, после этого добавляют в воронку 25 мл циклогексана, тщательно перемешивают смесь и затем промывают ее 10 мл 2 М едкого кали. После промывания смеси дают постоять и после разделения фаз нижнюю фазу отбрасывают. Циклогексановую фазу промывают двумя порциями по 10 мл 2 М раствора соляной кислоты и затем двумя порциями ( по 10 мл) щелочи. Окончательно смесь промывают 10 мл 2 М раствора соляной кислоты. После разделения фаз измеряют поглощение циклогексановой фазы при 253 нм в кювете с / 1 см, используя в качестве нулевого раствора холостой раствор. Концентрацию спирта в пробе определяют по предварительно полученному калибровочному графику. [10]
Исследована кинетика реакции ацилирования 4-амино - 4 -бромбифенила и 4-броманилина n - нитробензоилхлоридом в бензольном растворе. Полученные данные были сопоставлены с результатами изучения кинетики ацилирования аналогичных нитропроизводных 4-аминобифенила и анилина. [11]
В качестве модельных реакций были выбраны реакции ацилирования аминогруппы бензоилхлоридом, w - нитробензоилхлоридом и ацетилхлори-дом в бензольном растворе. Объектами исследования являлись анилин, и-нитроанилин, 4-аминобифенил, 4-амино - 4 -нитробифенил и 4-амино - 4 -нитро - 2 2 -диметилбифенил. [12]
Нитроантрацен 227 Нитроацетанилиды 79 Нитробензальдегиды 128, 133 и - Нитробензоат 179 п - Нитробензоилхлорид 175 Нитробензойные кислоты 152, 163, 169 Нитробензол 28, 63 ел. [13]
Из хлорангидридов ароматических карбоновых кислот наибольшее применение для ацилирования находит бензоилхлорид, а также n - нитробензоилхлорид. Используются, но в значительно меньших масштабах хлорангидриды м - и л-толуиловой кислог, л-хлорбензойной кислоты, 4-бифенилкарбоновой кислоты. [14]
Диазо-прочно-желтый 2G ( IG), получающийся при конденсации ( III) с одним молем - нитробензоилхлорида и одним моле-м / г - ( / - нитро) - бензамидобензоилхлорида с последующим восстановлением железом и кислотой, 7 8 обладает сродством к хлопку. [15]
Страницы: 1 2 3