Производный бензол
Cтраница 3
Уже для толуола стабильность тройного комплекса возрастает, поскольку последний разлагается на компоненты только при температуре выше 250 К - Все комплексы ксилола устойчивы даже при комнатной температуре. Это обусловлено возрастанием основности производных бензолов при увеличении числа метальных групп. [31]
Навеску 2 - 3 г винильного производного бензола или нафталина вносят в мерную колбу емкостью 100 мл, перемешивают и доводят до метки метанолом. [32]
Навеску 2 - 3 г винильного производного бензола или нафталина вносят в мерную колбу емкостью 100 мл, перемешивают и доводят до метки метанолом. [33]
Необычные свойства ароматического цикла объясняются тем, что в молекуле бензола двойные углерод-углеродные связи не находятся в фиксированных положениях. Это подтверждается существованием лишь одного изомера производного бензола с двумя одинаковыми соседними группами. [34]
Циклогексадиенильные катионы, образовавшиеся при протежировании ароматической системы, были изучены непосредственно. В принципе циклогексадиенильный катион, образовавшийся при протежировании производного бензола, может атаковать молекулу исходного непротонирован-ного соединения. Отрыв молекулы Н2 ( или гидрид-иона и протона) от такого димерного циклогексадиенильного катиона привел бы снова к образованию ароматической системы. Разрозненные примеры этого процесса, обычно в форме внутримолекулярной циклизации, известны уже много лет как реакция Шолля. [35]
 |
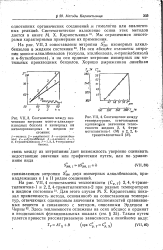
Зависимость гиперполярнзуемости ft молекул производных бензола от нх г. [36] |
Вычислив тем или иным способом цп или ju r для каждого заместителя, можно вычислять значения ( 3я систем с несколькими заместителями в предположении аддитивности вкладов заместителей. Очевидно, что для вычисления абсолютной величины гиперполяризуемости ляря-дизамещенного производного бензола в предположении выполнимости аддитивной схемы достаточно сложить абсолютные величины вкладов обоих заместителей или, что примерно то же самое, сложить абсолютные величины гиперполя-ризуемостей соответствующих монозамещенных. [37]
Были изучены и другие способы ускорения алкилирования и улучшения выходов. Далее выход может быть увеличен путем обработки высококипящих продуктов реакции бензолом и хлористым алюминием, тем самым превращая их в менее алкилированные производные бензолы. [38]
Количественные соотношения трех изомеров в получающихся двузамещенных продуктах меняются от случая к случаю в значительной степени и зависят от внешних условий, при которых проводится реакция замещения, например от температуры. В табл. 25 и 26 приведены данные об ориентирующем действии различных заместителей и о количественных соотношениях изомеров, образующихся при введении второго заместителя в молекулу однозамещенного производного бензола. [39]
На рис. VII, 3 сопоставлены энтропии S2g & изомерных алкил-бензолов в жидком состоянии Зо. На оси абсци сс отложены энтропии моно-н-алкилбензолов ( толуола, этилбензола, - пропйлбензола и н-бутилбензола), а на оси ординат энтропии изомерных им ме-тильных производных бензолов. [41]
Если не принимать во внимание вопросы, затронутые в разделе IV, А, то относительные величины, приведенные в табл. 15 для одного и того же соединения, должны характеризовать силу акцептора. Считают, что влияние акцептора не является постоянным фактором, поскольку в этом случае величины основности, полученные разными методами для одного и того же метильного производного бензола, были бы приблизительно постоянными. [42]
Неправильным Уэланд и Полинг считают и то, что Хюккель учитывает только один индуктивный эффект, тогда как следует принять во внимание также и резонансный эффект, вызываемый заместителем, а также и поляризацию молекулы производного бензола под влиянием атакующего реагента. В общем, однако, критикуя Хюккеля за эти допущения и неправильную интерпретацию результатов расчетов, Уэланд и Полинг в самой расчетной схеме Хюккеля по методу молекулярных орбиталей не видят ошибки и полагают, что ее можно развить, внеся некоторые поправки. [43]
Поскольку нитро - и карбоксигруппы являются жета-ориентантами, прямое нитрование, например бензойной кислоты, не приведет к искомому изомеру. Целесообразно применить толуол в качестве исходного производного бензола. Толуол нитруют в пара-положение, полученный п-нитротолуол отделяют от opmo - изомера, а затем окисляют метильную группу. [44]
Количественное рассмотрение данных по ароматическому замещению имеет весьма существенное значение как для понимания внутреннего механизма процесса, так и для предсказания результатов реакции. Важным шагом на этом пути явились исследования Ингольда [63, 64], в которых было введено представление о факторе парциальной скорости при замещении атома водорода бензола и его моносубституиро-ванных производных. Эта величина характеризует скорость замещения данного положения у производного бензола по отношению к реакционной способности каждого положения у незамещенного бензола. Для экспериментального определения указанного фактора используют конкурирующее замещение в смеси СбН6 и СбН5Х при действии какого-либо реагента. [45]
Страницы: 1 2 3 4