Бензофуроксан
Cтраница 2
У бензофуроксанов связь C-NO в промежуточном динитрозосоединении упрочняется благодаря сопряжению нитрозогруппы с бензольным кольцом. Поэтому лимитирующей стадией термораспада бензофуроксанов должно быть отщепление нитрозогруппы. Поскольку прочность связи C-NO определяется главным образом влиянием бензольного кольца и соседней иитрозогруппы, то влияние заместителей в бензольном кольце отходит на второй план, что видно из табл. 12 г. По данным авторов работы [562], константы скорости термолиза изученных бензофуроксанов в 27 раз меньше, чем у метилнитрофуроксана и в 55 раз больше, чем у самого стойкого из диалкилзамещенных фуроксанов - те тр а мети л енф урок-сана. [16]
Термораспад бензофуроксана начинается при т.пл. 70 - 71 С уже в твердой фазе и протекает со слабым тепловыделением до 186 С. В интервале 186 - 195 С происходит сильное экзотермическое разложение с тепловыделением 1896 18 кДж / кг или 257 2 кДж / моль. При 20б - 210 С деструкция практически завершается и остаток составляет 2 % от исходной массы. [17]
Для бензофуроксанов наиболее характерны свойства ароматических соединений. Так, бензофуроксаны легко вступают в реакции электро-фильного замещения, из которых особенно подробно изучена реакция нитрования. Легко также протекают реакции нуклеофнльного замещения групп, активированных электроотрицательными заместителями, причем, как и в ароматическом ряду, промежуточно образуются комплексы типа комплексов Мейзенгеймера. Далее, ннтробензофуроксаны, проявляя электроноакцепторные свойства, образуют тт-комплексы с ароматическими углеводородами. [18]
Способность бензофуроксана присоединять реагенты по двойным связям углеродного кольца рассматривается как указание на определенную хиноидность его структуры. [19]
Нитропроизводные бензофуроксана весьма склонны к образованию молекулярных тт-комплексов с ароматическими углеводородами н некоторыми их производными. Эту склонность проявляют и другие нитро-производные ароматического типа, из которых особенно выделяются в этом отношении 1 3 5-тринитробензол и 2 4 7-трннитрофлуоренон. [20]
Восстановление бензофуроксана в бензофуразан ( выход 40 %) наблюдалось также в процессе кипячения его в спиртовом растворе эквимольного количества этилата натрия при попытке осуществить в этих условиях реакцию бензофуроксана с азнном цнклогексанона [134] ( ср. [21]
Реакция бензофуроксанов с енамннами формально представляет собой 1 4-циклоприсоеднненне. [22]
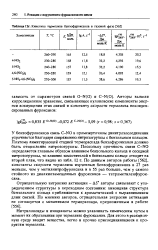 |
Кинетика термолиза бензофуроксанов в газовой фазе. [23] |
У бензофуроксанов связь C-NO в промежуточном динитрозосоединении упрочняется благодаря сопряжению нитрозогруппы с бензольным кольцом. Поэтому лимитирующей стадией термораспада бензофуроксанов должно быть отщепление нитрозогруппы. Поскольку прочность связи C-NO определяется главным образом влиянием бензольного кольца и соседней иитрозогруппы, то влияние заместителей в бензольном кольце отходит на второй план, что видно из табл. 12 г. По данным авторов работы [562], константы скорости термолиза изученных бензофуроксанов в 27 раз меньше, чем у метилнитрофуроксана и в 55 раз больше, чем у самого стойкого из диалкилзамещенных фуроксанов - те тр а мети л енф урок-сана. [24]
Термораспад бензофуроксана начинается при т.пл. 70 - 71 С уже в твердой фазе и протекает со слабым тепловыделением до 186 С. В интервале 186 - 195 С происходит сильное экзотермическое разложение с тепловыделением 1896 18 кДж / кг или 257 2 кДж / моль. При 206 - 210 С деструкция практически завершается и остаток составляет 2 % от исходной массы. [25]
Для бензофуроксанов наиболее характерны свойства ароматических соединений. Так, бензофуроксаны легко вступают в реакции электро-фильного замещения, из которых особенно подробно изучена реакция нитрования. Легко также протекают реакции нуклеоф ильного замещения групп, активированных электроотрицательными заместителями, причем, как и в ароматическом ряду, промежуточно образуются комплексы типа комплексов Мейзенгеймера. Далее, ннтробензофуроксаны, проявляя электроноакцепторные свойства, образуют тг-комплексы с ароматическими углеводородами. [26]
Способность бензофуроксана присоединять реагенты по двойным связям углеродного кольца рассматривается как указание на определенную хиноидность его структуры. [27]
Нитропроизводные бензофуроксана весьма склонны к образованию молекулярных тт-комплексов с ароматическими углеводородами н некоторыми их производными. Эту склонность проявляют и другие нитро-производные ароматического типа, из которых особенно выделяются в этом отношении 1 3.5 - тринвтробензол и 2 4 7-трннитрофлуоренон. [28]
Спектр бензофуроксана снимался при - 15 С; при повышении температуры сигналы сливаются. В спектрах всех остальных фуроксанов четкие отдельные пики видны уже при комнатной температуре. [29]
Предшественником бензофуроксана является N-хлорпроизводное. Действительно, для получения N-хлораминов широко применяется гипо-хлорит натрия. [30]
Страницы: 1 2 3 4