Нуклеаз
Cтраница 2
В случае высокомолекулярных РНК возможности метода серьезно ограничиваются значительной неспецифической деградацией полинуклеотидной цепи, наблюдающейся после пяти-шести циклов. Вероятными источниками ненативных концов служат примесные нуклеазы, а также неоптимальный выбор реагентов и экспериментальных условий. Проблема заключается в том, чтобы как можно полнее устранить эти причины и, таким образом, получить возможность однозначно анализировать более длинные участки цепи. [16]
Токсины-ферменты способствуют гидролитическому расщеплению отдельных структурных компонентов клеток: белков, нуклеиновых кислот, полисахаридов, липидов. Среди токсинов такого типа встречаются протеазы, нуклеазы, гиалуронидазы, фосфолипазы и др. - все они вызывают то или иное нарушение нормальных физиологических реакций человека или животного. [17]
Локализация других деполимераз автолитического комплекса различается у про - и эукариотных организмов. В клетках прокариот протеазы, амилазы, нуклеазы сосредоточены в цитозоле. В эукарио-тических клетках большая часть их находится в специализированных вакуолях - лизосомах. Как у тех, так и у других пусковая роль в деградации клеточных биополимеров отводится протеазам. [18]
Токсины-ферменты способствуют гидролитическому расщеплению отдельных структурных компонентов клеток: белков, нуклеиновых кислот, полисахаридов, липидов. Среди токсинов такого типа встречаются протеазы, нуклеазы, гиалуронидазы, фосфолипазы и др. - все они вызывают то или иное нарушение нормальных физиологических реакций человека или животного. [19]
Относительная доступность некоторых гомодезоксиполинуклеотидов дает возможность получать соответствующие олигодезоксинуклеотиды их ферментативной деградацией. Для этой цели используют ДНК-азу I и нуклеазу микрококков ( см. стр. [20]
Ошибки при использовании изоморфных производных, полученных путем замены иона металла, находящегося в нативном белке, на более тяжелые элементы, могут возникать из-за изменений в структуре металл-лигандных центров при замене металла. Кристаллографические исследования карбоксипептидазы А [29, 67], карбоангидразы С [68, 69] и нуклеазы стафилококка [33] показали, что более тяжелый ион металла смещен относительно металла в нативном белке, как и следовало ожидать, исходя из различных координационных свойств и ионных радиусов соответствующих металлов. Из-за вполне вероятного в этих условиях изменения конфигурации боковых цепей аминокислот, являющихся лигандами, отсутствие точного изоморфизма приводит к некоторой ошибке в расчете фаз. Эти изменения также могут привести к утрате точного изоморфизма. Вообще говоря, эта проблема может быть частично решена путем использования фаз, полученных для нескольких изоморфных производных. При расчете электронной плотности вблизи центра связывания металла для производного, в котором тяжелый атом замещает катион нативного белка, могут быть использованы фазы, определенные для других производных. [21]
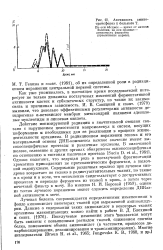 |
Активность амино. [22] |
Действие ионизирующей радиации в значительной степени связано с нарушением целостности макромолекул и систем, несущих информацию и необходимых для ее реализации в процессе жизнедеятельности организма. В радиационном поражении генома и его материальной основы ДНП-комплекса важное значение имеют высокоспецифичные протеазы и различные нуклеазы. В вилочковой железе, селезенке и других органах обнаружена высокоспецифичная по отношению к гистонам щелочная протеаза [ Suciu D. Однако полагают, что ведущая роль в постлучевой фрагментации хроматина принадлежит не протеолитическим ферментам, а щелочной эндонуклеазе. Содержание различных нуклеаз при лучевом синдроме возрастает не только в радиочувствительных тканях, но также и в крови и в моче, что несомненно свидетельствует о деструктивных процессах и переходе ферментов из тканей в кровь, а затем через почечный фильтр в мочу. По мнению Н. И. Керовай ( 1959), одним из тестов лучевого поражения может служить определение ДНКаз-ной активности в моче. [23]
Эти результаты показывают, что ингибиторное влияние катионов металлов обусловлено связыванием их вблизи центра координации Са ( П), а не неспецифическим связыванием другими участками белка. Особенно интересно сравнить влияние ионов Sr ( II) и Ва ( П) на нуклеазу стафилококка. Эти результаты показывают, что стереохимические требования к координации катиона металла при гидролизе РНК должны несколько отличаться от требований при гидролизе ДНК, поскольку Sr ( II) катализирует гидролиз ДНК, но не РНК. [24]
Токсическое действие соединений мышьяка объясняется их взаимодействием с сульфгидрильными группами ферментов, что ведет к снижению их активности и, следовательно, к нарушению биохимических процессов в организме. Так, соединения мышьяка блокируют фермент карбоксил азу, обеспечивающую окисление пиро-виноградной кислоты, снижают активность каталазы крови, инактивируют уреазу, нуклеазу и фосфатазу. Кроме того, под влиянием соединений мышьяка уменьшается выработка тиреотропного гормона передней доли гипофиза. [25]
Эта модель объясняла обнаруженное соотношение пяти гистоновых белков, находящихся в комплексе с ДНК, природу их агрегации и тот факт, что определенные нуклеазы расщепляют большую часть хроматина на блоки длиной около 200 пар оснований. Эта модель имеет основную структурную единицу, называемую нук-леосомой. Нуклеосома состоит из двух молекул каждого из гистоновых белков Н2А, Н2В, НЗ и Н4, ассоциированных с кольцевой ДНК, содержащей 200 пар оснований. Полагают, что лишь одна из четырех нуклеосом находится также в комплексе с негистоно-выми белками. Первые предположения заключались в том, что ДНК обернута вокруг внешней оболочки белкового кора нуклео-сомы, образующей глобулу ( 36), которая соединена с соседними глобулами свободной короткой ДНК. Эти тетрамеры могут открываться подобно книге, что позволяет осуществлять копирование ДНК без вытеснения гистоновых белков. Электронные микрофотографии хроматиновых зерен не позволяют выбрать более вероятную из этих моделей. [26]
В клетках ( как и в пищеварительном канале) нуклеиновые кислоты постоянно подвергаются атаке со стороны различных нуклеаз. Например, существенным фактором в регуляции синтеза белков является разрушение - как правило, довольно быстрое - информационных РНК-Хотя ДНК сама по себе очень устойчива, нуклеазы призваны вырезать поврежденные сегменты из одиночных цепей, что является важной частью процесса репарации ДНК ( гл. Таким образом, наблюдается активное расщепление полинуклеотидов на мононуклеоти-ды, гидролизуемые далее фосфатазами до нуклеозидов. [27]
Большинство ферментов находится внутри клетки. KJ точной стенки, например гидролазы целлюлозы и крахмал Эндоферменты чаще всего находятся в клеточных органоидг но могут быть и в цитоплазме, например ферменты, катализ рующие процесс брожения - фосфогексоизомераза, фосфогекс киназа, альдолаза, ферменты пентозного цикла, гидролити1 ские ферменты и др. Гидролитические ферменты, наприм протеазы ( катепсины), липазы, фосфатазы, нуклеазы, уча вующие в процессе автолиза клетки, локализированы в cnei альных органеллах - лизосомах. Полагают, что в бактери функцию лизосом несут мезосомы. [28]
Так, широко известная рибонуклеаза, являющаяся одним из наиболее простых белков-ферментов, гидролизует полимерную рибонуклеиновую кислоту ( РНК) вблизи от ее звена, несущего пиримиднновое основание. Нуклеазы играют важную роль в биосинтезе белков. [29]
Страницы: 1 2 3 4
