О-бис
Cтраница 2
Разрешение и информативность рассматриваемого метода могут быть существенно повышены, если анализируемые препараты перед собственно ГХ разделением предварительно обработать, например, М О-бис ( триметилсилил) ацетамидом. Достигаемое при этом количественное блокирование фенольных гндроксильных и метилольных групп позволяет свести к минимуму внутримолекулярное взаимодействие и за счет этого значительно повысить летучесть компонентов анализируемой пробы. [16]
После извлечения вредных примесей из воздуха стекловолокнистым фильтром собранные на нем ЛОС экстрагировали ме-тиленхлоридом в ультразвуковой бане, после чего к экстракту добавляли М О-бис ( триметилсилил) трифторацетамид, содержащий 1 % триметилхлор-силана. Экстракт фильтруют и концентрируют при комнатной температуре в токе азота. Анализ проводят на капиллярной колонке ( 30 м х 0 25 мм) с силиконом SE-30 при программировании температуры в интервале 70 - 250 С с использованием ПИД или кремнийселективного ПИД. [17]
По патентным данным, О О-диметил - 5 - 4-хлорфенилтиофос-фат, О О-диэтил - 5 - 4-хлорфенилтиофосфат, О О-бис - ( 2-хлорэтил) - S-4 - хлорфенилтиофосфат, О О-бис - ( 2-хлорэтил) - S-2 - нитрофенил-тиофосфат и их гомологи в 0 5 % - ной концентрации поражают большинство двудольных и однодольных растений. Более устойчивы к воздействию этих эфиров тиофосфорной кислоты бобы и хлопчатник [ 351, а О 0-диметил - 5 - 2-нитпофенилтиофосфат, О. [18]
Триметилсилилдиэтиламин ( ТМСДЭА) ( CH3) 3SiN ( C2Hs) 2 Диметилхлорсилан ( ДМХС) H ( CH3) 2SiCl Тетраметилдисилазан ( ТМДС) H ( CH3) 2SiNHSi ( CH3) 2H М О-бис - ( Триметилсилил) ацетамид - очень активный донор ТМС. Он взаимодействует со спиртами с образованием ТМС-эфи-ров, причем часто эта реакция протекает количественно при комнатной температуре. Столь же активным ТМС-донором является реагент БСТФА, используемый в тех случаях, когда побочные продукты агента БСА мешают анализу; моно ( триметилсилил) трифторацетамид и три-фторацетамид имеют меньшие времена удерживания, чем соответствующие нефторированные производные БСА. И БСА, и БСТФА чувствительны к действию влаги, и ни то, ни другое соединение не требует кислотного катализатора. Еще один силилирующий агент, ТСИМ, реагирует с гидроксильными группами, образуя лишь ТМС-эфиры спиртов, фенолов, органических кислот, окси-аминов, стероидов, флаванолов, гликолей, нуклеотидов, оксикис-лот и барбитуратов. Последние два агента силилирования из приведенного списка используют для образования диметилсилильных эфиров, которые более летучи, чем соответствующие ТМС-эфиры. [19]
Это экстрагирование позволяет повысить концентрацию анализируемого фосфата. Затем раствор смешивают с М О-бис ( триметилсилил) трифторацетамидом содержащим 1 % триметилхлорсилана и оставляют при комнатной температуре на 15 мин. Для анализа рекомендуется применять пламенно-ионизационный или пламенно-фотометрический детектор. [20]
В другой работе [13] для анализа водных растворов фосфатов рекомендуется применять предварительную колонку, в которой вода испаряется и остается остаток соли. Затем добавляют тот же реагент М О-бис ( триметил-силил) трифторацетамид, содержащий 1 % триметилхлорсилана. Для анализа применяют колонку, заполненную хромосорбом W, содержащим 5 % силикона SE-30, нагреваемую до 150 С. [21]
Произзодные получали обрабатывая оксистероиды и, о-бис - ( диметидизопропилсилил) трифторацетамидом в пиридине в течение 1 - 2 час. [22]
Обычно по водному способу технический тиофос получается с содержанием О О-диэтил - О-4-нитрофенилтиофосфата 85 - 92 %, по ацетоновому способу может быть получен препарат 98 % - ной чистоты. Основной примесью в техническом препарате являются О-этил - О О-бис - ( 4-нитрофенил) - тиофосфат, нитрофенол и небольшое количество триэтилтиофосфата. [23]
Обычно по водному способу технический тиофос получается с содержанием О О-диэтил - О-4-нитрофенилтиофосфата 85 - 92 %, по ацетоновому способу может быть получен препарат 98 % - ной чистоты. Основной примесью в техническом препарате являются О-этил - О О-бис - ( 4-нитрофенил) - тиофосфат, нитрофенол и небольшое количество триэтилтиофосфата. [24]
Период 50 % - ного исчезновения метилтиофаната на листьях яблони и винограда равен примерно 15 и 12 дням соответственно. В качестве ( продуктов метаболизма были выделены БМК и образующийся в результате реакции окисления о-бис ( М - карбокоиметилуреидо) бензол. [25]
Силиловые эфиры легко гидролизуются уже при длительном стоянии на воздухе, поэтому их желательно получать непосредственно перед масс-спектрометрическим анализом. Было показано [332], что триметилсилиловые эфиры при исследовании смесей спиртов могут быть получены непосредственно в ходе хромато-масс-спектрометрического анализа силилированием М О-бис ( триметилсилил) трифторацетамидом в колонке. [26]
Для подавления возможных побочных реакций олигомериза-ции и циклотримеризации моноалкина в качестве моноалкина предложено использовать бис ( триметилсилил) ацетилен. Триме-тилсилильные группы легко удаляются на более поздних стадиях. При использовании этого алкина диин медленно добавляют к кипящему бис ( триметилсилил) ацетилену ( растворитель), содержащему каталитическое количество дикарбонилциклопен-тадиенилкобальта; в этом случае с высоким выходом образуется о-бис ( триметилсилил) замещенный продукт. Алкин, используемый в качестве растворителя, легко можно выделить из реакционной смеси в чистом виде и использовать повторно. [27]
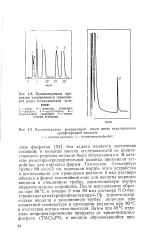 |
Хроматограммы продуктов хлорирования германиевой руды тетрахлоридом углерода.| Хроматограмма реакционной смеси после силилирования. [28] |
Эта задача является достаточно сложной, и попытки многих исследователей ее количественного решения вначале были безуспешными. После высушивания образца при 80 С в течение 3 мин 80 мкл раствора М О-бис - ( триметилсилил) трифторацетамида 1 % триметилхлор-силана вводили в реакционную трубку шприцем при комнатной температуре и проводили реакцию при 80 С в отсутствие потока газа-носителя. [29]
Благодаря высокой эффективности капиллярных колонок ( до 6000 теоретических тарелок на метр) менее важным становится фактор селективности. При существующей технологии деактиви-рования поверхности стеклянных колонок даже на неполярной фазе SE-30 возможно разделение высокополярных соединений. Таким образом, при применении высококачественных стеклянных капиллярных колонок с термостабильной универсальной фазой ( например, SE-30 или SE-54) отпадает необходимость тщательного подбора и периодической смены селективных фаз. Необходимо только систематически, раз в 3 - 5 месяцев, проводить, силилирование поверхности капиллярной колонки и интерфейса для уменьшения фона колонки и адсорбционных потерь. Силилирование осуществляется медленным вводом в хроматограф 5 мкл М О-бис ( триметилсилил) ацетамида или диметилдихлор-силана в изотермическом режиме при 140 С. [30]
Страницы: 1 2