Бериллид
Cтраница 1
Бериллидами называются химические соединения бериллия с металлами. Основные их свойства: стойкость против окисления при высоких температурах ( доходящих для отдельных бериллидов до 1400 С); высокая прочность на изгиб при повышенных температурах; хрупкость при комнатной температуре и для некоторых бериллидов - способность пластически деформироваться выше 1200 - 1300 С; высокие температуры плавления бериллидов редких тугоплавких металлов; высокая твердость. В настоящее время известны бериллиды для 40 элементов, причем установлено существование до 90 двойных бериллидных фаз и большого количества тройных и многокомпонентных фаз, содержащих бериллий. В табл. 66 приведены физические свойства некоторых наиболее тугоплавких бериллидов. [1]
Тугоплавкость бериллидов, легкость, прочность и устойчивость к окислению до 1650 С делают их идеальным конструкционным материалом Для ракет, управляемых снарядов и спутников. [2]
Защитное действие бериллидов от окисления обусловлено образованием плотного поверхностного слоя на основе окиси бериллия. [3]
При образовании бериллидов металлов подгруппы меди у атомов бериллия вновь проявляется стремление к образованию электронных / - конфигураций и соответственно - структурных элементов из атомов бериллия в решетках бериллидов. Это обусловлено наличием свободного s - электрона металлов, сравнительно легко передаваемого атомам бериллия. Поэтому медь легко образует бериллиды CuBe, CuBej и СйВе3, характеризующиеся нарастающим усложнением мотива атомов бериллия в кристаллических решетках. Более легкая отдача электрона атомом серебра содействует образованию ковалеитных связей между атомами бериллия и смещает содержание бериллия в соответствующих бериллидах в сторону более высоких значении. Еще большее число бериллидных фаз образует золото. В связи с повышением стабильности rf - состояний с ростом главного квантового числа при переходе от кальция к стронцию, барию и радию равновесие d s sp резко смещается в направлении образования конфигурации d - электронов, соответственно резко возрастают металлические свойства этих элементов. Характер химической связи в бериллидах редкоземельных металлов аналогичен связи в бериллидах щелочноземельных металлов вследствие близких потенциалов ионизации и наличия спаренных внешних s - электронов для всех лантаноидов. [4]
Химическая связь в бериллидах переходных металлов имеет ковалентно-ме-таллический тип. Доли типов связи в бериллидах переходных металлов обусловлены способностью d - оболочки металлов акцептировать или отдавать электроны с образованием тех или иных конфигураций локализованных электронов. [5]
Ниже приводятся некоторые данные по свойствам бериллидов, появившиеся недавно в печати. [6]
Содержание кобальта, никеля и бериллия, отвечающее бериллиду, значительно меньше при промывании водой, чем при промывании раствором азотнокислого аммония. Из таблицы следует, что содержание железа и хрома в анодном осадке после отпуска при 700 и 800 С соответствует карбиду тИе23Сб и сохраняется почтя постоянным независимо от состава промывной жидкости. После отпуска при 475 С содержание железа в анодном осадке увеличено вследствие изолирования вместе с карбидом хрома и остаточного аустенита. [7]
Из полученных результатов было рассчитано соотношение элементов в бериллиде ( в ат. [8]
При рассмотрении свойств карбидов, боридов, нитридов, силицидов, бериллидов и алюминидов преимущественное внимание уделено только высшим фазам диаграмм состояний соответствующих систем, так как именно эти фазы обычно образуются в поверхностном слое при одном из основных методов получения покрытий - диффузионном, в значительной степени определяя конечные свойства покрытия. [9]
Для бериллия довольно характерно образование с некоторыми другими металлами соединений ( бериллидов), обычно содержащих относительно много атомов Be. Последнее из этих соединений находит использование в качестве источника нейтронов. [10]
Соединения неметаллов и полуметаллов с бериллием только условно могут быть названы бериллидами. Так, электроотрицательность неметаллов и некоторых полуметаллов значительно выше электроотрицательности бериллия. [11]
На поверхности молибденовых и вольфрамовых образцов при всех температурах отжига образовывались многофазные диффузионные зоны из бериллидов МеЕе2, МеВе12 и др., а на ниобии - также многофазные, но наибольшую толщину имела фаза NbBe12, образование которой в основном и приводит к росту слоя. [12]
Нечто подобное мы наблюдаем в химии углерода, для которого АЯ образования нитридов, боридов, бериллидов и литидов близки друг к другу, но все же в химии углерода имеются два заведомо побеждающих элемента - кислород и фтор, вытесняющие все другие. [13]
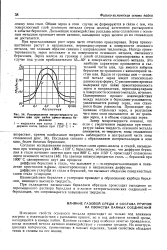 |
Распределение микротвердости по ширине шва при пайке армко-железа бериллием. [14] |
При охлаждении насыщенных бериллием образцов происходит выпадение из пересыщенного раствора бериллия в сс-железе интерметаллических соединений - бериллидов, что сопровождается повышением твердости. [15]
Страницы: 1 2 3 4