Облако - л-электрон
Cтраница 1
Облако л-электронов в молекуле, согласно Багдасарьяну, мо-делир ется как совокупность соприкасающихся шаров. Центры шаров расположены на серединах - связей, а диаметры равны межатомным расстояниям. Плотность электронов внутри шаров считается одинаковой. Число электронов в отдельных шарах равно сумме всех л-электронов. Эти числа электронов входят в уравнения, выражающие: 1) электростатическую энергию отталкивания электронных шаров друг от друга; 2) электростатическую энергию притяжения я-электронных шаров положительно заряженными остовами и 3) кинетическую энергию л-электронов. Расчет ведется в трех предположениях относительно взаимного отталкивания я-электронов внутри шаров: это отталкивание равно: 1) нулю, 2) половине электростатической энергии отталкивания и 3) последней с некоторыми поправками. [1]
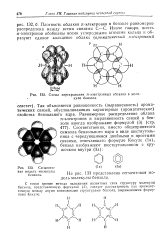 |
Схема перекрывания я-электронных облаков в моле - куле бензола.| Сегменте - ( la ( За. [2] |
Плотность облаков л-электронов в бензоле равномерно распределена между всеми связями С-С. [3]
 |
Схема перекрывания л-электронных облаков в бензоле.| Сегментовая модель молекулы бензола. [4] |
Плотность облаков л-электронов в бензоле равномерно распределена между всеми С-С - связями. Следовательно, л-электроны обобщены всеми углеродными атомами кольца, образуя единое кольцевое облако шести электронов ( ароматический электронный секстет); это условно показано схемой II. Таким образом объясняется равноценность ( выравненность) ароматических связей, придающих бензольному ядру характерные ( ароматические) свойства. [5]
При повороте осей симметрии облаков л-электронов соседних атомов на 90 по отношению друг к другу перекрывание облаков полностью прекращается, что означает фактический разрыв в этом месте цепи сопряжения. Однако и меньшее нарушение плоскостного строения, которое не приводит к полному прекращению перекрывания соседних л-электронных облаков и полному разобщению участков цепи сопряжения, лежащих по обе стороны от места нарушения параллельностей осей симметрии л-электронных облаков, сказывается на поглощении света: Ямакс сдвигается в сторону более коротких волн. [6]
Таким образом, в молекуле нафталина облако л-электронов менее симметрично, чем в бензоле. Связи 1 2; 3 4 в нафталине в некоторой степени аналогичны сопряженной системе связей в 1 3-бутадиене. [7]
Таким образом, в молекуле нафталина облако л-электронов менее симметрично, чем в бензоле. Связи 1 2 и 3 4 в нафталине в некоторой степени аналогичны сопряженной системе связей в 1 3-бу-тадиене. [8]
 |
Схематическое изображение молекулы диметилксилидина. [9] |
Нарушение копланарности молекулы приводит к отсутствию перекрывания облаков л-электронов и невозможности передачи электронных влияний. Известна, например, высокая реакционная способность пара-положения диметиланилина по отношению к электрофильным реагентам. Если, однако, в орто-положе-нии к диметиламинной группе ввести две метильные группы, то такой диметилксилидин уже не реагирует с азотистой кислотой. [10]
Такое смещение сопровождается уменьшением степени взаимного перекрывания облаков л-электронов в направлении двойной связи, снижением энергетических затрат ( энергии активации) на раскрытие этой связи и ее поляризацию, в результате чего повышается реакционноспособность мономера. [11]
Такое смещение сопровождается уменьшением степени взаимного перекрывания облаков л-электронов в направлении двойной связи, снижением энергетических затрат ( энергии активации) на раскрытие этой связи и ее поляризацию, в результате чего повышается реакционноспособность мономера. [12]
 |
Образование л-связей в молекуле бутадиена-1 3 за счет перекрывания 2р - орбиталей. [13] |
Взаимодействие двух или нескольких соседних л-связей с образованием единого облака л-электронов, в результате чего может легко происходить передача взаимовлияния атомов этой системы, как известно, называется эффектом сопряжения. Этот эффект способствует понижению общей энергии молекулы. Поэтому диены с сопряженными двойными связями - довольно устойчивые системы. [14]
 |
Схема методов получения бензола. [15] |
Страницы: 1 2 3