Облако - л-электрон
Cтраница 2
Реакции бензола ( рис. 28.3) обычно включают атаку электрофила на облако л-электронов. [16]
СС и особенно СС обладают большими поляри-зуемостями, делается вывод об относительно диффузном облаке л-электронов этих связей. [17]
Малые длины связей между кайносимметричными и немногослойными атомами С позволяют совершаться перекрыванию облаков л-электронов, а потому для химии углерода весьма характерны кратные связи в отличие от химии кремния. Эти связи настолько прочны ( этому способствует заметно и энергия корреляции) и вместе с тем в отсутствие катализаторов и высоких температур настолько мало реакцион-носпособны ( достаточно вспомнить необходимость платинового катализатора при гидрировании этиленовых производных), что органическая химия богата мономерами даже среди класса ненасыщенных соединений, молекулы которых могли бы полимеризоваться с разрывом кратных связей, если бы при помощи катализаторов была преодолена их инертность. Напомним, что и молекулы СО для своего сгорания в кислороде требуют катализаторов. Этилен полимеризуется при низких давлениях и температурах лишь в присутствии катализаторов, например, смеси триэтилалюминия и четы-реххлористого титана. [18]
Как известно, в силу sp - гибридизации, а также более высокой симметрии облака л-электронов ацетиленовая связь менее реакционноспособпа и прочнее двойной связи. [19]
Поскольку эти облака симметричны относительно осей, перпендикулярных линий а-связи, а в ароматических соединениях - относительно осей, перпендикулярных плоскости кольца, то максимальное перекрывание облаков л-электронов наблюдается при параллельном расположении их осей симметрии, что возможно лишь при плоском строении молекулы. Искажение плоскостности молекулы нарушает параллельность осей симметрии я-электронов облаков и уменьшает степень их взаимного перекрывания, нарушая взаимодействие л-электронов и возможность их смещения по цепочке сопряженных двойных связей. [20]
В некоторых случаях заниженные значения частот валентных колебаний ОН у ненасыщенных спиртов объяснялись [43] эффектами сте-рических затруднений, обусловленными наличием it - электронов, но возможно, что в этих случаях осуществляется водородная связь с облаком л-электронов. [21]
Для одной неподвижной фазы влияние дипольного момента компонента на величину теплоты растворения мало заметно. Облако л-электронов фуранового цикла не позволяет осуществлять свободного вращения атомов углерода и легко поляризуется. На примере хроматографического поведения тетрагидрофурилового и фурилового спиртов показано участие л-электронов двойных связей фуранового цикла. Наличие дипольного момента по двойной связи и хорошая поляризуемость позволяют ненасыщенным фура-новым соединениям образовывать более сильную связь с полярными соединениями по сравнению с насыщенными гомологами. [22]
Так объясняется равноценность ( выравненность) ароматических связей, обусловливающих характерные ( ароматические) свойства бензольного ядра. Равномерное распределение облака л-электронов и выравненность связей в бензоле иногда изображают формулой ( 3) ( стр. [23]
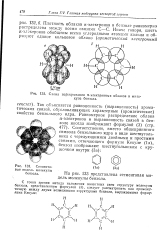 |
Схема перекрывания я-электронных облаков в молекуле бензола.| Сегменто - Са ( За. [24] |
Так объясняется равноценность ( выравненность) ароматических связей, обусловливающих характерные ( ароматические) свойства бензольного ядра. Равномерное распределение облака л-электронов и выравненность связей в бензоле иногда изображают формулой ( 3) ( стр. [25]
Двойная или тройная связь в эфире кротоноиой пли тетроловой кислоты проявляет А1 - эффект; введение этих связей в молекулу повышает электронную плотность на карбонильном углероде. При этом ацетиленовая группировка действует сильнее, так как здесь облако л-электронов может перекрываться с карбонильной функцией в любом положении ( ср. Эффект олефиновой или ацетиленовой группы в этих соединениях не проявляется, так как он компенсируется / - эффектом метилыюй группы, расположенной в конце системы. Это становится ясным при рассмотрении данных, полученных для эфира акриловой кислоты; здесь, помимо мезомер-ного ( М -) эффекта, полностью проявляется некомпенсированный индуктивный ( - / -) эффект двойной связи, и поэтому акриловый эфир гидролизуегся легче, чем эфир кротоновои кислоты. Рассмотренные влияния показаны в табл. 51 с помощью стрелок. [26]
Реакционноспособность соединений с кратными связями зависит от заместителей при двойной связи. Несимметричное положение электрофидь-ного заместителя при двойной связи ( CI, F, - OR) приводит к смещению облака л-электронов в направлении заместителя, и двойная связь поляризуется. В молекулах диалкилпроизводных, например изобутилене, электроны отталкиваются метальными группами. [27]
В пользу линейной конфигурации говорит то, что при этом взаимное отталкивание молекул NO наименьшее. Однако в случае реакции с кислородом 2NO O22N02 аргументом в пользу прямоугольной модели является то, что при этом может осуществиться сильное перекрывание облаков л-электронов молекулы О2 и валентного электрона каждой из молекул NO. Заметим:, что ни в одном из этих случаев активированный комплекс не имеет циклической конфигурации. [28]
Особый интерес представляют люминесцентные возможности ароматических соединений. Первым представителем этого ряда является бензол, обладающий шестью 0-связями, осуществляемыми о-электронами, направленными вдоль осей, соединяющих атомы, и обладающими круговой симметрией относительно этих осей, и тремя я-связями, осуществляемыми л-электронами, причем облака л-электронов размещены существенно отличным образом, нежели в случае о-связей. [29]
На самом же деле в бензоле нет обычных пар л-электронов, фиксированных между двумя определенными С-атомами, как это изображает схема I. В шести-членном цикле бензола все простые связи С-С и С - Н ( а-связи) лежат в одной плоскости. Облака л-электронов всех С-атомов, имеющие фррму объемных восьмерок, направлены перпендикулярно плоскости бензольного кольца. Каждое из таких облаков перекрывается облаками двух соседних С-атомов. [30]
Страницы: 1 2 3