Гибридное облако
Cтраница 1
Гибридные облака, как одноименно заряженные, электростатическими силами расталкиваются на максимальное расстояние друг от друга. При наличии четырех орбиталей ( как в молекуле СН4) они располагаются под углом 109 5 друг к другу. Такой угол говорит о том, что электронные орбитали атома углерода направлены к вершинам тетраэдра, а ядро атома С находится в центре его. [1]
Гибридные облака выступают наружу больше, чем р-облака, и образуют особенно прочные о-связи при обобщении с s - облаками четырех атомов водорода. Вообще, энергия связи всегда тем больше, чем полнее перекрываются в пространстве связывающие атомные состояния. В этом заключается принцип максимального перекрывания. [2]
 |
Схемы, показывающие образование химических связей в молекулах Na ( а и СОг ( б.| Схема, показывающая образование химических связей в молекуле С6Нв ( показаны только три р-облака. [3] |
Три гибридных облака образуют о-связи под углом 120 с двумя соседними атомами углерода и с атомом водорода. [4]
 |
Схемы образования химических связей в молекулах N2 ( a. [5] |
Два гибридных облака каждою углеродного атома образуют связи под углом 180, поэтому все четыре атома ( 2С и 2Н) расположены на одной прямой. Связь в молекуле ацетилена между углеродными атомами оказывается тройной: одна а - и две я-связи. [6]
Число образующихся гибридных облаков соответствует числу электронов, участвующих в гибридизации. Такой вид гибридизации называется sp - гибридизацией. [7]
 |
Расположение гибридных облаков в атоме. [8] |
Симметричное расположение гибридных облаков относительно ядра атома закономерно для любого вида гибридизации. В таблице 32 показано взаимное расположение осей гибридных электронных облаков при различных видах гибридизации. Каждая стрелочка передает направление оси одного из облаков. [9]
Образование четырех одинаковых, равноценных гибридных облаков происходит только в тех случаях, когда в результате химического взаимодействия образуются четыре совершенно одинаковые валентные связи. Например, в метане, в четыреххлористом углероде все четыре гибридные облака, участвующие в образовании связей, одинаковы и состоят из J / 4 s - облака и 8 / 4 р-облака. [11]
 |
Перекрывание атомных орбиталей. а - тип s - s ( Н - Н. б - тип s - sps I H - С. [12] |
Связи образуют и гибридные облака атома углерода. Например, во фрагменте С - Н образуется о - связь между гибридизованной орбиталью углерода и ls - орбиталью атома водорода ( рис. 10, б), а во фрагменте С - С - между двумя гибриди-зованными орбиталями ( рис. 10, в), о - Связь обладает большой прочностью, так как основная масса электронной плотности сосредоточена в небольшом пространстве между ядрами атомов. [13]
Три 5р2 - гибридных облака образуют три 0-связи. [14]
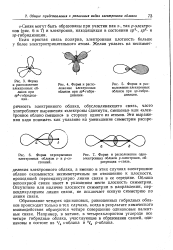
На рис. 5.4 показана форма гибридного облака, образовавшегося при комбинации облаков s - и р-электронов. [15]
Страницы: 1 2 3 4 5