Область - перекрывание - электронное облако
Cтраница 2
Как уже говорилось, я-связи менее прочны, чем а-связи, так как область перекрывания электронных облаков лежит в стороне от оси ветви. Это приводит к тому, что соединения с кратными связями значительно более реакционноспособны, чем соответствующие алканы. [16]
Вследствие меньшего размера атомов щелочноземельных металлов по сравнению с атомами щелочных металлов, область перекрывания электронных облаков не будет так сильно сдвинута в связевой области в сторону галогена, а потому степень ионности связи будет уменьшена. [17]
Неполярная связь - это ковалентная связь между атомами с одинаковой электроотрицательностью ( ЭО); при образовании неполярной связи область перекрывания электронных облаков находится на одинаковом расстоянии от ядер обоих атомов. [18]
Если атом А обладает достаточной энергией для того, чтобы, несмотря на растущие силы отталкивания, сближение продолжалось и область перекрывания электронных облаков увеличивалась, то это сближение поведет к такому уменьшению плотности электронного облака между ядрами атомов Б и В, которое будет равносильно исчезновению связи между ними. [19]
Каждая связь О - Н является полярной связью, так как ЭО ( О) ЭО ( Н); области перекрывания электронных облаков смещаются к атому кислорода, на котором возникает избыточный отрицательный заряд. На атомах водорода возникают избыточные положительные заряды. [20]
 |
Молекулярные термы окиси бериллия. [21] |
Рассматривая гра-фик, следует помнить, что 4т - и 1л - орби-тали уже являются молекулярными и связевыми и тут наблюдаются области перекрывания электронных облаков. Взаимное возмущающее их действие ведет к снятию вырождения и к расщеплению орбиталей. [22]
Электронные облака атомов имеют определенную пространственную ориентацию. Соответственно и область перекрывания электронных облаков находится в определенном направлении по отношению к взаимодействующим атомам. Поэтому ковалентная связь обладает направленностью. Характер распределения электронной плотности при образовании связи зависит от вида взаимодействующих атомов. [23]
 |
Энергия некоторых связей. [24] |
Электронные облака атомов имеют определенную пространственную ориентацию. Соответственно и область перекрывания электронных облаков находится в определенном направлении по отношению к взаимодействующим атомам. Поэтому ковалент-ная связь обладает направленностью. Характер распределения электронной плотности при образовании связи зависит от вида взаимодействующих атомов. [25]
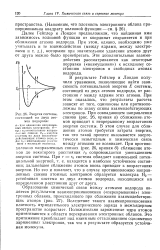 |
Энергия системы, состоящей из двух атомов водорода. [26] |
Вследствие такого взаимопроникновения плотность отрицательного электрического заряда в межъядерном пространстве возрастает. Положительно заряженные ядра атомов притягиваются к области перекрывания электронных облаков. Это притяжение преобладает над взаимным отталкиванием одноименно заряженных электронов, так что в результате образуется устойчивая молекула. [27]
Вследствие такого взаимопроникновения плотность отрицательного электрического заряда в межъядерном пространстве возрастает. Положительно заряженные ядра атомов притягиваются к области перекрывания электронных облаков, что и приводит к образованию устойчивой молекулы. [28]
Вследствие такого взаимопроникновения плотность отрицательного электрического заряда в межъядерном пространстве возрастает. Положительно заряженные ядра атомов притягиваются к области перекрывания электронных облаков. Это притяжение преобладает над взаимным отталкиванием одноименно заряженных электронов, так что в результате образуется устойчивая молекула. [30]
Страницы: 1 2 3
