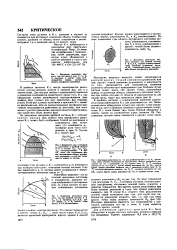
Область - двухфазное равновесие
Cтраница 3
Приступая в математической обработке результатов ТЭ для построения Р - Т и Т - х проекций БС, исследователь располагает таблицей опытных данных, включающей набор составов, давлений, температур в областях двухфазных равновесий, и Р i - Т i таблицей моновариантных равновесий. [31]
Например, изоконцентраты с постоянным содержанием магния в богатой магнием части системы А1 - Mg-Zn ( см. рис. 47, б) будут пересекать различные коноды, для которых состав одной, а в области двухфазного равновесия и обеих фаз будет непрерывно изменяться. Поэтому и диаграмма состав - свойство не может подчиняться закону механической смеси. [32]
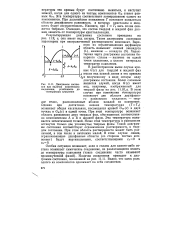 |
Диаграммы состояния при наличии химического соединения, устойчивого до температуры плавления. [33] |
Ож станет равным GTT, Эта температура соответствует затвердеванию одного из компонентов. При дальнейшем понижении Т начинают появляться области двухфазного равновесия, в которых кристаллы и жидкость будут сосуществовать. [34]
 |
Внутреннее строение надсолндусной части физико-химической фигуры плавкости тройной системы простого эвтектического типа. [35] |
Выше ликвидуса располагается однофазная жидкая область тройной системы. Между тремя поверхностями ликвидуса и линейчатыми поверхностями располагаются области двухфазных равновесий Ж А, Ж В и Ж С. [36]
К, критич точка менее летучего компонента В; заштрихована область двухфазного равновесия газ газ. [38]
Линия tBabcdtA на рис. 63 представляет собой линию ликвидус диаграммы; линия tBa b c d tA - линию солидус. Область, заключенная между линией солидус и линией ликвидус, соответствует области двухфазного равновесия жидкости и кристаллов твердого раствора. [39]
Для того чтобы изотропная фаза обладала устойчивостью относительно виртуальных изменений плотности, необходимо выполнение условия ( др / дУ) 0, где р - давление; V-удельный объем вещества. Этому условию удовлетворяют не только стабильные состояния жидкости и пара, но и метастабильные состояния, проникающие в область двухфазного равновесия. Примером может служить перегретая жидкость. [40]
На ранних стадиях разработки промышленной технологии выращивания кристаллов кварца было распространено мнение, согласно которому неструктурную примесь в синтетическом кварце отождествляли с тяжелой фазой - продуктом расслоения гидротермального щелочного раствора. В какой-то мере подобная точка зрения была связана с выводами авторов работы [15], которые на основании экспериментальных данных построили рГ - диаграмму четырехкомпонентной ( SiO2 - N326 - СО2 - Н2О) существенно водной системы, определяющую область двухфазного равновесия для двух значений концентрации содового раствора. Согласно этим данным, в области достаточно высоких давлений ( при температурах промышленного синтеза) можно вести перекристаллизацию в условиях, при которых не будет происходить расслоение рабочего раствора и, следовательно, растущие кристаллы не будут захватывать продукты расслоения. [41]
На ранних стадиях разработки промышленной технологии выращивания кристаллов кварца было распространено мнение, согласно которому неструктурную примесь в синтетическом кварце отождествляли с тяжелой фазой - продуктом расслоения гидротермального щелочного раствора. В какой-то мере подобная точка зрения была связана с выводами авторов работы [15], которые на основании экспериментальных данных построили рГ - диаграмму четырехкомпонентной ( SiCb - Na2U - ССЬ - Н2О) существенно водной системы, определяющую область двухфазного равновесия для двух значений концентрации содового раствора. Согласно этим данным, в области достаточно высоких давлений ( при температурах промышленного синтеза) можно вести перекристаллизацию в условиях, при которых не будет происходить расслоение рабочего раствора и, следовательно, растущие кристаллы не будут захватывать продукты расслоения. [42]
Исследованы равновесия жидкость-кристалл и жидкость - жидкость в системе никлододекан-водные растворы уксусной кислоты с содержанием воды от 0 8 до 18.2 % при температурах 20 - 200 С. Показано, что до Г 0ЭС в системе существует равновесие жидкость-кристалл, а выше 50 С образуются две жидкие фазы. Область двухфазного равновесия жидкость-жидкость сильно расширяется с увеличением содержания воды в уксусной кислоте. [43]
Если образуются две различные кристаллические формы у одного из компонентов, существующие при разных температурах, и непрерывный ряд твердых растворов со вторым компонентом образует высокотемпературная форма р первого компонента, то температура перехода этой формы в низкотемпературную форму или температура полиморфного превращения [ З а обычно понижается при добавках второго компонента. В равновесии с жидкостью участвует в этом случае только высокотемпературная форма. Область двухфазного равновесия р а образуется в диаграмме состояния двумя спускающимися к оси составов диаграммы линиями, как на рис. 22, исходящими из точки А превращения чистого вещества. [44]
 |
Изотермы растворимости. Система вода - дегазированная нефть Долинского месторождения. [45] |
Страницы: 1 2 3 4