Беркеит
Cтраница 1
Беркеит 180 Бикарбонат аммония 66, 79 ел. [1]
Беркеит ( 2Na2SO4 - Na2CO3) представлен твердыми растворами переменного состава. [2]
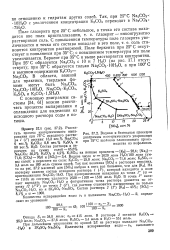 |
Водная и безводная проекции диаграммы изотермического упаривания при 75 С щелоков глиноземного производства из нефелинов. [3] |
Поле беркеита при 25 С отсутствует и появляется при 35 С; с повышением температуры это поле увеличивается. Беркеит при 35 С и выше растворяется конгруэнтно. [4]
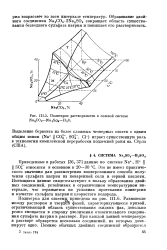 |
Политерма растворимости в солевой системе Na2CO3 - Na2S ( 4 - Н20. [5] |
Выделение беркеита из более сложных четверных систем с одним общим ионом ( Na COg, SO, Cl -) играет существенную роль в технологии комплексной переработки подземной рапы оз. [6]
Судьба кристаллов беркеита связана с их растворением и разделением двух солей. [7]
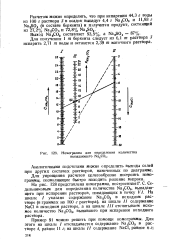 |
Номограмма для определения количества выпадающего Na2CO3. [8] |
Для получения 1 т беркеита следует из 6 1 т раствора 3 испарить 2 71 т воды и останется 2 39 т маточного раствора. [9]
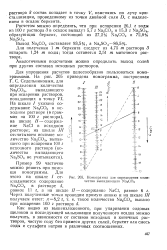 |
Номограмма для определения количества выпадающего Na COg. [10] |
Для получения 1 т беркеита следует из 4 75 т раствора 3 испарить 1 24 т воды; тогда останется 2 51 т маточного раствора. [11]
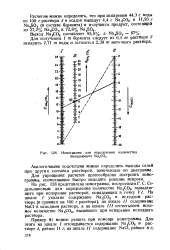 |
Номограмма для определения количества выпадающего Na2CO3. [12] |
Для получения 1 т беркеита следует из 6 1 т раствора 3 испарить 2 71 т воды и останется 2 39 т маточного раствора. [13]
 |
Изотерма 20 системы Na. CO-Na. SO - NaCl-H 0. [14] |
Выше температуры 26 1 появляется двойная соль беркеит - 2Na2S04 Na2C03, поле которой увеличивается с повышением температуры и выше 30 занимает большую часть диаграммы. [15]
Страницы: 1 2 3 4