Беркеит
Cтраница 4
При упаривании исходного раствора 2 его состав изменяется по кривой 7 - 1 / 7 до точки VI, причем в осадок выпадает смесь солей Na2CO3 - H2O и беркеита. [46]
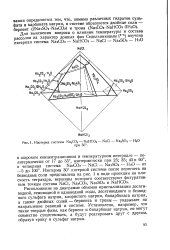 |
Изотерма системы Ыа2С03 - ЫаНСО3 - NaCl - Na2SO4 - Н2О. [47] |
Расположение на диаграмме объемов кристаллизации десяти-водной, семиводной и одноводной соды, десятиводного и безводного сульфата натрия, хлористого натрия, бикарбоната натрия, а также двойных солей - беркеита и троны - указывает на направление реакций в системе. Установлено, например, что такие твердые фазы, как беркеит и бикарбонат натрия, не могут совместно существовать, а будут реагировать друг с другом, образуя трону и сульфат натрия. [48]
Из этих данных можно определить, что для получения 1 т моногидрата в первом цикле следует выпарить 2 62 т воды, а для получения 1 т смеси моногидрата и беркеита во втором цикле - 1 73 т воды. [49]
Из этих данных можно определить, что для получения 1 т моногидрата в первом цикле следует выпарить 2 62 / га воды, а для получения 1 т смеси моногидрата и беркеита во втором цикле - 1 73 т воды. [50]
Как видно из вышеизложенного, при упаривании содовых щелоков и последующей кальцинации полученного осадка можно получить, в зависимости от составов исходных и конечных растворов, чистую соду без примеси других солей, беркеит или смесь соды и сульфата натрия в различных соотношениях. [51]
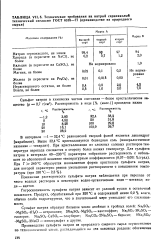 |
Технические требования на натрий сернокислый технический согласно ГОСТ 6318 - 77 ( производство из природного сырья. [52] |
Сульфат натрия образует большое число двойных и тройных солей: Na2SO4 - MgSO4 4Н2О - астраханит; 3Na2SO4 MgS04 - вантгоффит ( Na2SO4 3K2SO4 - глазерит; Na2SO4 - CaSO4 - глауберит; Na2CCv2Na2SO4 - беркеит; 9Na2SO4 - MgSO4 - 3NaCl - нонасульфат и другие. [53]
Составы природных содовых растворов определяются фигуративными точками, расположенными близко к углу Na2CO3 ( например точка /), на линии совместной кристаллизации солей ( например, точка 2) или в поле двойной соли беркеита ( например, точки 3 и 4) - При концентрировании таких растворов состав их будет изменяться по лучу, проведенному из угла Na2CO3 или из точки D, отвечающей составу двойной соли, с выделением в осадок Na2C03 Н 20 до кривой насыщения. [54]
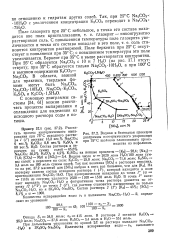 |
Водная и безводная проекции диаграммы изотермического упаривания при 75 С щелоков глиноземного производства из нефелинов. [55] |
Поле беркеита при 25 С отсутствует и появляется при 35 С; с повышением температуры это поле увеличивается. Беркеит при 35 С и выше растворяется конгруэнтно. [56]
 |
Общая схема переработки межкристальной рапы оз. Серлз процессом Трона. [57] |
ЗРабота выпарной установки обеспечивает выделение поваренной соли в основном в виде крупных кристаллов. Беркеит же и литий-натрий фосфат образуют мелкие кристаллы, выносимые из классификатора со сливом в отстойник для беркеита. [58]
Для вывода 1 т сульфата натрия в виде беркеита расходуют 0 4 т кальцинированной соды. Если беркеит не используется, то на 1 т NaaSO4, выведенного из рассола, теряется 1 т NaCl и 0 1 т NaOH. [59]
Для вывода 1 т сульфата натрия в виде беркеита расходуют 0 4 т кальцинированной соды. Если беркеит не используется, то на 1 т Na2SO4, выведенного из рассола, теряется 1 т NaCl и 0 1 т NaOH. [60]
Страницы: 1 2 3 4