Обмен - кислород
Cтраница 2
Реакции обмена кислорода на галогены и другие группы. Альдегиды и кетоны при взаимодействии с РС15 обменивают атом кислорода на два атома хлора, что используется для получения геминальных дихлоралканов ( оба атома хлора присоединяются к одному и тому же атому углерода, стр. [16]
Изучение обмена кислорода между Со О з и меченым растворителем Н О показало, что 6 из 12 атомов кислорода обмениваются гораздо быстрее, чем остальные. Однако все 12 атомов кислорода в Сг ( СаО4) з являются эквивалентными и обмениваются намного быстрее, чем расщепляется комплекс. [17]
Скорость обмена кислорода в решетке Со3О4 оказывается значительно больше, чем в оксиде меди и в шпинели-хромите цинка, что указывает на большую подвижность кислорода в этом оксиде. [18]
Другие возможности обмена кислорода здесь не рассматриваются. [19]
Основные закономерности обмена кислорода были установлены А. И. Бродским и его школой. [20]
Основные закономерности обмена кислорода были установлены А. И. Бродским и его школой. [21]
Изучение реакции обмена кислорода неорганических солей дает ценные сведения об относительной прочности связи атомов кислорода с неметаллическими атомами аниона. [22]
Выяснено, что обмен кислорода сопровождает гидролиз циклического этиленфосфата только в кислом, но не в щелочном растворе. На основании этих фактов удалось сделать примерный набросок геометрии переходного состояния реакций гидролиза и обмена этих эфиров ортофосфорной кислоты в кислой среде. [23]
Осуществленные исследования реакций обмена кислорода не позволяют определить энергии диссоциации моноокисей, так как дают только разности этих энергий. Для одного из окислов приходится принимать энергию диссоциации, полученную другими методами. [24]
Было проверено отсутствие обмена кислорода между U04 и гидратирующей водой как при приготовлении соединения, так и при его сушке. [25]
Так как скорости обмена кислорода решетки и обмена на поверхности сравнимы, следует считать, что энергия связи кислород - металл важна для каталитических процессов окисления. Из окислов наиболее активны окислы переходных металлов с 3, 4, 8 и 9 d - электронами в катионах, и теплоты превращения высших окислов в низшие, например V5 - - V4 или Со3О4 - - СоО, служат хорошими ориентировочными данными для оценки каталитической активности. [26]
Хотя точный механизм кислотно-катализируемого обмена кислорода окспанионов не известен, бесспорно ясно, что присоединение протона к аниону ХО Г значительно повышает скорость обмена кислорода с водой растворителя. Этого и следовало ожидать, так как независимо от механизма связь X - О должна быть прочнее в X - О, чем в X - ОН. Почти такое же поведение наблюдалось для гидролиза моноалкилъных офи-ров фосфорной кислоты; в этом случае Ш) РО3Н - является наиболее реакцион-носпособпой частицей. [27]
Как уже отмечалось, обмен кислорода и углекислого газа; между альвеолярным воздухом и кровью капилляров, покрывающих стенку альвеол, основан на законах диффузии молекул газа из области более высокого парциального давления в область более низкого давления. Па ( 7 мм рт. ст.), в результате чего молекулы ССЬ переходят из крови в альвеолы. Следует отметить, что при спокойном дыхании процесс диффузии в легких здорового человека происходит весьма быстро, в результате-парциальные давления кислорода и углекислого газа в капиллярах легких и в альвеолярном воздухе практически одинаковы. [28]
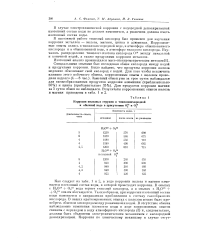 |
Коррозия железных стружек в тяжелокислородной. [29] |
Специальными опытами был исследован обмен кислорода между водой и продуктами коррозии. Было найдено, что продукты коррозии железа медленно обменивают свой кислород с водой. Для того чтобы исключить влияние этого побочного обмена, коррозионные опыты с железом проводили недолго ( 4 - 8 час. [30]
Страницы: 1 2 3 4