Обмен - бром
Cтраница 3
Для доказательства строения бромпроизводное обрабатывали - бутиллитием. Образовавшееся а результате обмена брома на металл литиевое производное при разложении метанолом дало 1 2-бензодифенилен. Положение атомов брома в 3-бром - 1 2-бензодифенилене было доказано встречным синтезом этого соединения. [31]
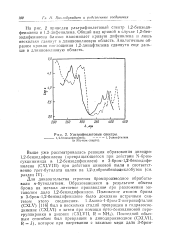 |
Ультрафиолетовые спектры. [32] |
Для доказательства строения бромпроизводное обрабатывали н-бутиллитием. Образовавшееся в результате обмена брома на металл литиевое производное при разложении метанолом дало 1 2-бензодифенилен. Положение атомов брома в 3-бром - 1 2-бензодифенилене было доказано встречным синтезом этого соединения. [33]
 |
Конфигурации алкильных групп в переходных состояниях реакций бимолекулярного замещения. [34] |
Оценив вначале, исходя из геометрии молекул и переходных состояний, расстояния между несвязанными отталкивающимися атомами, затем по формуле, приведенной в гл. Эти данные для реакций обмена брома приведены в табл. 117 в строке, обозначенной & Н ( пространств. [35]
Примерами двух типов нуклеофильного замещения являются рассмотренные на стр. При действии на это соединение ионов ОН ( в концентрированной щелочи) происходит обмен брома на гидроксил по механизму 5 2 с вальденовским обращением. [36]
Примерами двух типов нуклерфильного замещения являются рассмотренные на стр. При действии на это соединение ионов ОН ( в концентрированной щелочи) происходит обмен брома на гидроксил по механизму 5к / 2 с вальденовским обращением. [37]
Должно, однако, заметить, что Торпе, на основании своих опытов, отвергает общность этого вывода. Упомяну еще об одном следствии, которое мне кажется возможным вывести из приведенных чисел Густавсона, если они далее оправдаются хоть в тесной границе. Если СВг4 нагревать с RC14, то происходит обмен брома хлором. Судя по величине атомных весов В 11, С 12, Si 28, около 11 % хлора заменяется бромом. [38]
На обмен брома в K2 [ PtBre ] свет оказывает заметное влияние. Так, при концентрации K2 [ PtBr6 ] 0.55 - 10 - 2 мол / л и концентрации КВг 3.3 - 10 - 2мол / л ( t - 20, время обмена 30 мин. Последнее обстоятельство связано, возможно, с неодинаковой освещенностью в опытах. Влияние света на обмен брома в K2 [ PtBre ] подлежит дальнейшему исследованию. [39]
Имеется много доказательств правильности этих предположений. Де Брайн и Штегер [77] показали, что скорость щелочного гидролиза метил - и этилио-дидов в водном этиловом спирте уменьшается с увеличением содержания воды. Хыоз [78] установил, что скорость гидролиза тиретп-бутилхлорида ( не зависящая от прибавления щелочи) с увеличением содержания воды в спирте увеличивается. Ле Ру и Сегден [79] показали, что скорость обмена брома между бромид-ионом ( из бромистого лития) и н-бутилбромидом в ацетоновом растворе уменьшается при добавлении к раствору 10 % воды. Дейвис и Льюис [80] установили, что скорости присоединения диэтиланилина и некоторых арилдиэтилфосфинов к йодистому этилу в ацетоновом растворе увеличиваются при добавлении 10 % воды. Меншуткин [29] показал, что присоединение триэтиламина к йодистому этилу протекает быстрее в спиртах, чем в углеводородах. [40]
В водный раствор тиаминбромида загружают роданистый аммоний и при температуре 60 С водным аммиаком доводят рН до 9 0, кристаллизуют и высушивают. Полученный тиаминроданат растворяют в 7 % - ном НС1, очищают активированным углем и пропускают через колонку со специально подготовленным анионитом. В колонке происходит ионный обмен CNS на С1 и в элюате получают водный раствор тиаминхлорида, который выделяют очисткой углем, сгущением в вакууме и кристаллизацией. Преимущества данного метода заключаются в его высоком эффекте очистки тиамина от посторонних примесей в результате выделения его через промежуточное соединение тиаминроданат. В практике нашел применение способ превращения тиаминбромида в тиаминхлорид через тиаминроданат и ионный обмен, хотя более технологичным является метод превращения бромида в хлорид реакцией обмена в среде метилового спирта или фенола, насыщенных хлористым водородом. Однако вопрос о способе осуществления реакции обмена брома на хлор в бромаминопиримидине требует дополнительных технико-экономических исследований. Во всяком случае решение этого вопроса в пользу метода через тиаминроданат является преждевременным. [41]
Майером пространственными затруднениями в реакциях карбоксильной группы в ортпо-дизамещенных бензойных кислотах ( в отличие от гомологов фенилуксусной кислоты) можно было бы предполагать более значительные пространственные затруднения в бимолекулярных реакциях трет-бутилгалогенидов, содержащих галоген ближе к месту разветвления, чем в соответствующих неопентилгалогенидах, где галоген находится на один атом дальше от места разветвления. Однако такая аргументация ошибочна. Сделанный выше противоположный вывод основан на том, что в первую очередь геометрия переходного, а не нормального состояния молекулы важна для объяснения пространственного замедления. Подобные расчеты были произведены и для других пар входящих и уходящих галогенов. На первый взгляд может показаться странным, что рассчитанные величины, характеризующие пространственное отталкивание, не сильно зависят от размеров входящих и отщепляющихся групп, которые могут быть и не идентичными, хотя расчеты гораздо легче сделать в случае одинаковых групп. Причина этого заключается в компенсирующих факторах. Так, если в реакции обмена брома бромид-ион заменить на иодид-ион, то больший галоген в переходном состоянии будет находиться дальше от центрального атома углерода, и поэтому все расстояния между атомом иода и несвязанными с ним атомами будут увеличиваться. Однако из-за больших размеров иодид-иона допустимые пределы расстояний, ниже которых отталкивание становится значительным, также увеличиваются. В результате этого отталкивание остается примерно одинаковым и энергии отталкивания имеют одинаковый порядок величины, Так, величина АЯ ( пространств. [42]
Страницы: 1 2 3