Протонный обмен
Cтраница 3
Имеющиеся сведения о кинетике процессов протонного обмена охватывают практически все классы молекул, способных образовывать водородные связи. В сочетании с методом остановленной струи [11] она позволяет исследовать протонный обмен в растворах ( рис. 2.11) даже в тех случаях, когда полупериод обмена составляет всего несколько миллисекунд. [31]
Лучшее понимание механизма молекулярных процессов протонного обмена может быть достигнуто в результате дальнейшего спектроскопического изучения циклических комплексов, определения их времен жизни, исследования динамики последовательных стадий процесса при помощи различных физических и химических методов и теоретических расчетов потенциальных поверхностей взаимодействия. [32]
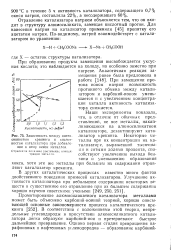 |
Зависимость между интенсивностью крекинга и кислотностью катализатора при добавлении к нему окиси металлов. [33] |
При замещении протона ионом натрия возможность протонного обмена между катализатором и карбоний-ионом уменьшается и с увеличением концентрации металла активность катализатора снижается. [34]
В зависимости от константы равновесия kt протонного обмена между исходными кислотой и щелочью и константы скорости &2 из этой схемы следуют [9] различные предельные кинетические результаты. Вообще можно установить зависимость между свободной энергией активации переноса протона и константой равновесия или изменением стандартной свободной энергии суммарного кислотно-основного равновесия, как, например, в случае электропроводности в водно-спиртовых растворах сильных кислот; это соотношение известно под названием правило Брен-стеда. Недавние кинетические исследования, выполненные методом ЯМР [242], указывают на наличие зависимости между константами скоростей протонного обмена и рКл органических кислот, действующих как акцепторы протонов, донорами которых в метаноле являются метоксониевые ионы. [35]
Преобладающее влияние протонодонорной способности на скорость протонного обмена не совсем понятно. Эти факты могут рассматриваться как указание на влияние уменьшения протоноакцепторной способности атома А в группе АН, а также на циклическую структуру промежуточных комплексов протонного обмена. Следует отметить, что в отличие от спиртов и алифатических аминов повышение протонодонорной способности дифениламина и N-алкиланилинов определяется не индуктивным эффектом, а сопряжением неподеленной пары электронов атома N с тг-электронами цикла. [36]
В то время как константы скорости протонного обмена для систем спирт - спирт и спирт - амин в СС14 имеют значения порядка 100 - 400 л / ( моль с), константы скорости протонного обмена между аминобораном и метанолом или вторичными аминами в том же растворителе оказываются на 3 - 4 порядка ниже. Этот результат указывает на то, что промежуточный комплекс имеет циклическую, а не линейную структуру. [37]
Как было показано в [5, 6], скорость протонного обмена в системах с Н - связями зависит от протонодонорной и протоноакцепторной способности молекул-партнеров. Выбор в качестве одного из объектов метилмеркаптана определяется, во-первых, малой прочностью Н - связей, - образуемых группой SH и как донором и как акцептором протона, и, во-вторых, высокой упругостью его паров в рабочем интервале температур. Равновесное распределение изотопов водорода между группами ОН и SH устанавливается за десятки секунд и более [7, 8], поэтому запуск процесса при смешивании реагентов может быть осуществлен простыми средствами. Кроме того, для регистрации кинетики в этом временном интервале пригодна стандартная инфракрасная аппаратура. [38]
Кислотами называются соединения, которые в результате протонного обмена с водой могут образовать ион гидроксония. [39]
Некоторые растворители могут привести к уменьшению скорости протонного обмена. Так, при наличии нескольких гидро-ксильных групп взаимный обмен приводит к образованию единой линии ОН группы в спектре. При растворении в димешлсульфо-ксиде отдельные ОН группы стабилизируются водородными связями с этим растворителем. При этом взаимный обмен прекращается и удается обнаружить неэквивалентные ОН группы соединения. [40]
Было высказано мнение [33], что кинетика протонного обмена в подобных системах определяется кооперативным переносом протона в промежуточном комплексе. Для протонного обмена между спиртами, аминами и водой, который, по-видимому, тоже характеризуется кооперативным механизмом, константы скорости k значительно больше, а энергии активации ЛЕ близки к значению энергии активации диффузии. На основании изучения кинетического изотопного эффекта в системе метанол - вода в СС14 Бурейко и др. [12] пришли к выводу, что скорость протонного обмена определяется стадией образования циклического комплекса. Этот процесс может протекать очень медленно из-за чрезвычайно низкого значения константы равновесия. Хотя в этом случае скорость реакции не лимитируется диффузией, энергия активации может действительно определяться диффузией. Проблему лимитирующей стадии в различных механизмах процессов протонного обмена еще предстоит исследовать в дальнейшем. [41]
О важной роли водородной связи в кинетике протонного обмена свидетельствуют также результаты изучения влияния на этот процесс растворителей, способных образовывать водородно-связанные комплексы с рассматриваемыми молекулами. Этот вопрос обсуждался в работе [37] с учетом динамических свойств водородной связи ( см. разд. Это можно объяснить тем, что наличие разветвленной сети водородных связей в бинарных смесях препятствует образованию циклических комплексов между молекулами спирта и воды. [42]
При исследовании роли водородной связи в процессах протонного обмена большое значение имеет рассмотрение механизма реакции и его лимитирующей стадии. Приведенные выше данные согласуются с предположением, что первая стадия протонного обмена включает перенос протона в циклическом промежуточном комплексе. Чтобы образовался такой комплекс, атомы А и В должны иметь неподеленные пары электронов. Изучение методом ЯМР систем амин - динитроэтан показало, что перенос протона в них происходит быстро, а скорость протонного обмена мала. [43]
Дан обзор современного состояния спектроскопических исследований процессов некаталитического протонного обмена в молекулярных системах с водородной связью. Изложены основные закономерности, наблюдающиеся при изучении скорости протонного обмена для различных классов молекул. [44]
Вопросу о роли водородных связей в реакциях протонного обмена типа АН ВН - АН - f - ВН посвящена обзорная статья С. Ф. Бурейко, Е, В. Авторы подробно рассмотрели влияние водородных связей на скорость реакции и ее механизмы. Совокупность экспериментальных данных согласуется с предположением, что обмен протонами происходит в циклическом комплексе, образованном двумя водородными связями. Такая модель призвана объяснить большую скорость реакции и низкую энергию активации. Следует, однако, отметить, что кинетика этих процессов в целом исследована еще недостаточно. Например, оказалось, что константа скорости протонного обмена между НС1 и НВг в результате тщательной очистки системы сильно понизилась, что свидетельствует о наличии неконтролируемых примесей, катализирующих процесс. [45]
Страницы: 1 2 3 4