Электронная оболочка
Cтраница 3
Электронные оболочки большинства стабильных молекул напоминают оболочки инертных газов, поэтому энергии электронного возбуждения этих молекул очень велики, и полосатые спектры их лежат в далекой ультрафиолетовой части спектра. Электронные же уровни большого числа нестабильных молекул и свободных радикалов, таких как ОН, NH, GN, лежат сравнительно невысоко, и спектры их наблюдаются в легко доступной кварцевой ультрафиолетовой области. Именно эти нестабильные соединения труднее всего количественно анализировать химическим путем. Спектроскопические методы в ряде случаев позволяют количественно измерить концентрации этих неустойчивых промежуточных веществ и изучить их изменение во времени. Преимуществом метода является также отсутствие влияния измерений на ход реакции или процесса горения, тогда как химический анализ иногда требует прекращения реакции на различных стадиях для отбора проб. [31]
Электронную оболочку хлороводорода можно рассматривать в нулевом приближении как суммарное облако иона С1 -, в котором как бы потонул до известной глубины протон. Чтобы изобразить радиальные функции исходного аниона, можно ограничиться лишь a - орбиталями, так как 2л -, хотя и заполнены, но являются в принципе несвязевыми. Хотя они слегка отражаются своим присутствием на энергии связи, но настоящих л-связей не образуют; это характерно для всех соединений водорода. [32]
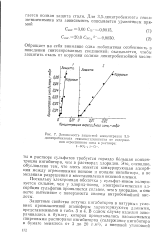 |
Зависимость защитной концентрации 3 5-динитробензоата гексаметпленимина от содержания агрессивного нона в растворе. / - so2. -. 2 - е. -. [33] |
Поскольку электронная оболочка у сульфат-ионов поляризуется сильнее, чем у хлорид-ионов, электростатическая адсорбция сульфатов проявляется сильнее, чем у хлоридов, и они легче вытесняют с поверхности анионы нитробензойной кислоты. [34]
Две электронные оболочки, ответственные в основном за отталкивание, мало отличаются от оболочек атомов соседних элементов второго периода периодической системы. Неудивительно, что значение А, с точностью до коэффициента 3, совпадает с результатом расчета Леннард-Джонса [47] для константы отталкивания двух атомов неона в газовой фазе. [35]
Их электронные оболочки с отрицательными зарядами притягиваются положительно заряженной пластиной и немного смещаются в ее сторону. А положительно заряженные ядра атомов притягиваются и смещаются к отрицательно заряженной пластине конденсатора. Происходит, как говорят, поляризация атомов и молекул диэлектрика: в нем возникает электрическое поле. Причем, это электрическое поле внутри диэлектрика направлено противоположно полю пластин, так как положительные полюса молекул направлены в сторону отрицательной пластины, а отрицательные - в сторону положительной. Поэтому добавочное поле уменьшает главное. Оно как бы частично нейтрализует заряды пластин. А от этого источник тока может подать на пластины конденсатора новые заряды. В результате емкость конденсатора увеличивается. Это свойство диэлектриков называется их диэлектрической проницаемостью. Она различна у разных материалов: у бумаги в 3 - 3 5 раза, а у слюды даже от 4 до 7 5 раза больше, чем у вакуума ( безвоздушного пространства), проницаемость которого принята за единицу. [36]
Эта электронная оболочка заряжена отрицательно, а поверхность металла вследствие обеднения ее электронами - положительно. Следовательно, возникает сила, притягивающая электрон и мешающая ему выйти. [37]
Поэтому электронная оболочка таких атомов или ионов имеет сферическую симметрию. [38]
Две электронные оболочки, ответственные в основном за отталкивание, мало отличаются от оболочек атомов соседних элементов второго периода периодической системы. Неудивительно, что значение Л, с точностью до коэффициента 3, совпадает с результатом расчета Леннард-Джонса [47] для константы отталкивания двух атомов неона в газовой фазе. [39]
Именно электронные оболочки ответственны за химические и многие физические ( в частности, оптические) свойства вещества. Это связано с тем, что электроны могут теряться атомом и присоединяться к нему, образуя положительно и отрицательно заряженные ионы. Кроме того, они могут переходить с одного энергетического уровня на другой, в результате чего атом будет испускать или поглощать кванты света. Электрон - родоначальник класса лептонов, который соцержит и другие частицы. [40]
Именно электронные оболочки ответственны за химические и многие физические ( в частности, оптические) свойства вещества. Это связано с тем, что электроны могут теряться атомом и присоединяться к нему, образуя положительно и отрицательно заряженные ионы. [41]
Поскольку электронные оболочки перекиси водорода заполнены, то, чтобы сделать ее способной к захвату новых электронов, необходимо предварительное расщепление молекулы. Точно так же, чтобы создалась возможность отдачи электрона или деления его, вероятно, требуется разрыв молекулы. После этого основное внимание концентрируется на более своеобразном или единственно реакциоиноспособном осколке. В реакции ( 25) - это ион НО, нуклеофильная или электронодонорная частица. Гидроксилышй свободный радикал, вероятно, нужно считать элек-троноакцепторной частицей, тогда как пергидроксильпый свободный радикал может играть роль и акцептора и донора электронов. Тобольский и Месробян ( см. работу [40], стр. [42]
Заполнение электронных оболочек у последующих 18 элементов ( Rb - Хе) аналогично / заполнению электронных оболочек уже рассмотренных 18 элементов 4 периода ( К - Кг): вслед за Rb ( 5s) и Sr ( 5s2) на протяжении декады Y ( 4d) - Cd ( 4d10) с несколькими провалами комплектуется 4с / - оболочка, затем последовательность, нарушается и элек-фоны поступают в р-оболочку 5-го слоя, хотя свободна вся 4 / - оболочка. [43]
Деформируемость электронной оболочки сказывается и на оптических свойствах веществ. Поглощение лучей связано с возбуждением внешних электронов. Электронные переходы отвечают тем меньшим энергиям, чем более поляризуема частица. Если частица малополяризуема, то возбуждение требует больших энергий; им отвечают ультрафиолетовые лучи. Если атом ( ион) легко поляризуется, то возбуждение требует квантов небольшой энергии; им отвечает видимая часть спектра. В этом случае вещество оказывается окрашенным. Таким образом, наряду с веществами, цвет которых обусловлен окраской содержащихся в них ионов, существуют окрашенные соединения, образованные бесцветными ионами, окраска которых является результатом межионного взаимодействия. [44]
Деформируемость электронных оболочек, а следовательно, и молекулярная рефракция, являются важным критерием, характеризующим многие физические и химические свойства вещества. [45]
Страницы: 1 2 3 4