Образование - 0-связь
Cтраница 1
Образование 0-связей обусловлено участием одного валентного электрона от каждого атома С и N, причем каждый атом С и N, за исключением атомов углерода метальных групп, образует по три о-связи. Остальные шесть я-электронов ( включая неподеленную пару р-электронов атома азота) находятся в поле молекулярных остовов положительно заряженных атомов углерода и азота. Таким образом в молекуле красителя, так же как и в куске металла, я-электрон можно рассматривать, как если бы он находится в одномерном потенциальном ящике, стенки которого были бы бесконечно высоки. Длина цеп молекулы красителя, в качестве модели которой можно взять молекулу полиена, равна длине ящика L Nl, где / - длина звена НС СН - СН, N - число звеньев в цепочке, равное числу пар подвижных я-элект-ронов. [1]
В образовании 0-связей с атомами хлора и кислорода в молекуле SOC12 участвуют три р-электрона атома серы, следовательно, молекула SOC12 имеет пирамидальную структуру. [2]
 |
Структура графита. [3] |
В образовании 0-связей участвуют три электрона каждого атома углерода. Четвертый электрон внешнего слоя занимает 5 -орбиталь, не участвующую в гибридизации. [4]
 |
Структура графита. [5] |
В образовании 0-связей участвуют три электрона каждого атома углерода. Четвертый электрон внешнего слоя занимает 2р - орбиталь, не участвующую в гибридизации. [6]
Перенос заряда при образовании 0-связи М - СО и я-связи М - СО приводит к уменьшению порядка связи в молекуле СО. [7]
Орбиты не могут быть использованы для образования 0-связей, так как максимум электронной плотности у них располагается вдоль биссектрисы угла. [9]
 |
Асимметрическая полимеризация эфиров непредельных кислот. [10] |
Второй тип катализатора индуцирует асимметрию в первом звене без образования 0-связи между диссимметрическим агентом в катализаторе и цепью. [11]
Лиганды, в которых донорный атом содержит пару электронов, способных к образованию 0-связи, и низко энергетическую вакантную я-разрыхляющую орбиталь, которая может принять за счет дативной связи пару электронов от атома металла. [12]
В комплексе регибридизация молекулярных орбиталей ацетилена из sp - в 5р2 - состояние приводит к образованию новых углерод-углеродных 0-связей. [13]
Более низкоэнергетичная связывающая я-орбиталь в, основном состоянии содержит оба электрона, не участвующие в образовании 0-связей. [14]
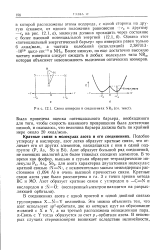 |
Схема инверсии в соединениях NR3 ( текст. [15] |
Страницы: 1 2 3 4
