Образование - 0-связь
Cтраница 2
Это можно объяснить тем, что азот использует 5р 2-орбитали, две из которых идут на образование 0-связей с X и Y, а на третьей расположена неподеленная пара, я - Связь с Y тогда образуется за счет р2 - орбитали азота. [16]
 |
Образование коорди. [17] |
Лиганды, в соединениях с которыми металлы проявляют низкие степени окисления, способны отдавать заряд металлу при образовании 0-связи и получать обратно часть или весь заряд при образовании координационных я-связей металл - - лиганд; такими лигандами являются СО, NO, CN - и RNC. Эти четыре лиганда имеют высокую силу поля и расположены в конце спек-трохимического ряда. Поэтому они вызывают существенное расщепление d & - и dy - орбиталей и приводят к большой энергии стабилизации поля лигандов в комплексах. Переходные элементы - это слабо основные металлы, так что при образовании комплекса следует ожидать переноса заряда до тех пор, пока ионы металла не станут почти электронейтральными. Таким образом, металлы в высоких степенях окисления будут образовывать устойчивые комплексы с лигандами, которые отдают иМ часть заряда при образовании координационной ст-связи. С теми лигандами, которые для образования сильной связи требуют национной я-связи между 3d - op - также возникновения я-связей биталью атома металла и раз-металл-лиганд, устойчивые комплексы образовываться не будут, так как это повышает положительный заряд металла. С другой стороны, образование я-связи металл - лиганд важно для получения устойчивых комплексов металлов с низкими степенями окисления, так как при этом лиганду возвращается основная часть заряда, отданного металлу при образовании 0-связей, что делает металл почти нейтральным. [18]
В присутствии слабого основания ( карбонат - или ацетат-иона) происходит нуклеофильная атака одной из координированных двойных связей с образованием 0-связи металл - углерод. Если двойные связи не идентичны, то реагирует более напряженная. В бицик иче-ских системах нуклесфил подходит с зкзо-стороны, и реакция проходит как стереоспецифическое трокс-присоединение, благодаря тому, что металл уже координирован в эн о-положении. В этом состоит отличие от ртути, которая образует л-комплекс с экзо-стороны, поскольку образование бис-олефинового комплекса в случае Hg не дает дополнительного выигрыша энергии. [19]
 |
Энергетическая диаграмма эдск-трофильного присоединения к алкенам. [20] |
Стр В алкенах три из четырех валентных электронов атома углерода ( 2s, 2px, 2pv) участвуют в образовании 0-связей с атомами водорода или углерода. Орбиталь четвертого электрона имеет гантелеобразную форму и ориентирована перпендикулярно по отношению к плоскости, в которой находятся 0-связи. Перекрывание двух р-орбиталей соседних атомов приводит к образованию я-связи, расположенной перпендикулярно плоскости о-связей. [21]
Каждый из атомов углерода в кольце бензола находится в состоянии р2 - гибридизации и затрачивает по три валентных электрона на образование 0-связей с двумя соседними атомами углерода и с одним атомом водорода. Каждое из таких р-электронных облаков перекрывается над и под Плоскостью кольца с р-электронными облаками двух соседних атомов углерода. Плотность облаков я-электронов в бензоле равномерно распределена между всеми связями С - С. Так объясняется равноценность ( выравненность) ароматических связей, обусловливающих характерные ( ароматические) свойства бензольного ядра. [22]
Здесь, однако, различие легко объяснимо, так как в случае нафтенов этот вид изомеризации связан с разрывом ц образованием 0-связей, а в случае олефинов - с разрывом и образованием я-связей. [23]
 |
Схема перекрывания t2s ( dxy - орбитали центрального атома с sg ( p - групповыми орбиталями лигандов в плоскости ху. [24] |
Групповые орбитали t u имеют подходящую симметрию, чтобы перекрываться с / и-орби-талями центрального атома, но последние уже использованы для образования 0-связей. [25]
Так, например, при связывании с двумя атомами углерода метильных групп и образовании дийетилового эфира СН3 - О - СН3 атом кислорода может использовать четыре зр3 - гибридных орбитали: две для образования 0-связи за счет перекрывания с зр3 - орбиталями каждого из двух атомов углерода, а остальные две - для оставшихся свободными двух пар электронов. Было показано, что угол С-О - С составляет 110, длина связи С-О равна 1 42 А, а ее энергия 86 ккал / моль. [26]
Вероятность образования при ионизации I фосфорорганического аниона должна расти с ростом электрофильности радикала R, так как при этом электронное облако оттягивается с атома фосфора и d - орбитали его становятся более способными к образованию 0-связей. [27]
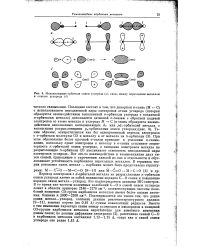 |
Молекулярные орбитали окиси углерода ( а. связь между переходным металлом и окисью углерода ( б. [28] |
Таким образом, осуществляется как бы одновременный переход электронов с 0-орбитали молекулы СО к металлу и от металла на я-орбитали СО. При этом образование более прочной 0-связи приводит к усилению я-связы-вания, поскольку сдвиг электронов к металлу в а-связи усиливает акцеп-торность я-орбиталей окиси углерода, а смещение электронов металла на разрыхляющие л-орбитали СО увеличивает основность неподеленной пары электронов углерода. Вот это-то взаимодействие и взаимовлияние двух типов связей, приводящее к упрочнению каждой из них в отдельности и обусловливает устойчивость карбонилов переходных металлов. В терминах теории резонанса связь металл - карбонил может быть представлена структурами: М - С О МС0 [9-11] или М - CsO - MC0 [2] и др. Переход электронов с d - орбиталей металла на разрыхляющие я-орбитали окиси углерода влечет за собой понижение порядка С-О связи и повышение порядка связи металл-углерод. [29]
Гибридные орбитали вытянуты к вершинам правильного тетраэдра. Перекрывание таких атомных орбиталей ведет к образованию 0-связей. [30]
Страницы: 1 2 3 4