Образование - катион-радикал
Cтраница 3
Хиршлер и Хадсон [73] высказали, однако, предположение, что на алюмосиликате превращение перилена с образованием катион-радикала может происходить на бренстедовском центре с участием одной из форм хемосорбированного кислорода как акцептора электронов. [32]
Поскольку приложенный потенциал слишком низок для окисления цианид-иона, то первоначальной реакцией будет окисление субстрата, приводящее к образованию катион-радикала. Последующие стадии включают присоединение цианид-иона, перенос второго электрона и потерю протона, однако не ясно, в какой момент времени происходит атака цианид-ионом. [33]
Если следовать постулату о последовательном переносе электронов [18], то первичный электродный процесс при прямом окислении углеводорода представляет собой образование катион-радикала ( уравнение 13 1) Однако вследствие высокой химической активности катион-радикалов обычно протекает быстрая реакция с нуклеофилами и ( или) основаниями, присутствующими в электролите, которая приводит к образованию либо продукта присоединения катион-радикала к иуклеофилу ( уравнение 13.2), либо продукта элиминирования протона от катион-радикала путем переноса его к основанию ( уравнение 133) Образующиеся продукты являются нейтральными радикалами В некоторых случаях потенциал окисления образовавшегося ради кала менее положителен. [34]
Поскольку окислительные потенциалы дитиановых производных карбонильных соединений намного выше, чем окислительные потенциалы ТТА, равновесие переноса электрона сдвинуто в сторону образования катион-радикала ТТА. Быстрая реакция разрыва связи С - S смещает равновесие в сторону продуктов. Гидролиз и вторая стадия окисления затем приводят к карбонильному соединению, освобожденному от защитной группы. В реакции катализатор не расходуется, что указывает на длинную каталитическую цепь. Химический метод с использованием стехиометрического количества гексахлорантимоната катион-радикала ТТА приводит к аналогичным результатам. Прямое снятие 1 3-дитиановой и 1 3-дитиолановой защиты было описано в разд. [35]
Исключительная стабильность органических катион-радикалов в трифторуксусной кислоте [88] или в смеси сорастворителей трифторуксусная кислота - дихлорметан [89] позволяет остановить реакцию на стадии образования катион-радикала, получаемого из продукта сочетания. После окисления полярность электродов изменяют на обратную и электрохимическая реакция протекает далее как восстановление этих катион-радикалов до бифенилов. [36]
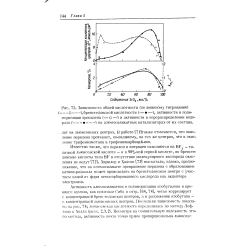
Полученные значения 5 и J ( таблица 5) согласуются с установленной окисления метальных групп I ( ГТ и МВФ и подтверждают факт образования катион-радикала. [37]
При действии урадиад на замороженные при - 196 С растворы 0 005 моль / л ароматических аминов ( дифениламин, трифениламин) в смеси метилциклогексана и изопентана происходит образование катион-радикалов аминов, которые могут быть идентифицированы по их спектрам поглощения в видимой области. Сяектрофотометрирование должно производиться при температуре жидкого азота, так как при нагревании раствора до комнатной температуры происходит необратимое исчезновение катион-радикалов. [38]
На том основании, что спиновая интенсивность уменьшается после восстановления катализатора в водороде, Фого высказал предположение, что следы кислорода в адсорбенте действуют как сильные электронные акцепторы при образовании катион-радикалов из адсорбированных полиаценов и, следовательно, фениламинов и других соединений. Количественная оценка концентрации кислорода, удаляемого с поверхности алюмосиликагеля, выполненная Холлом [85], показала, что количество кислорода, удаленного восстановлением в водороде, равно 3.3 - 1012 атомов кислорода на 1 см2 поверхности. Это очень близко к поверхностной концентрации парамагнитных радикалов, для которых она равна 2 - Ю12 атомов на 1 см2 для случая перилена. Более того, в том случае, когда кислород частично удален, уменьшение количества катионов перилена соответствует отношению: 1 катион на 1 атом кислорода. Эти результаты свидетельствуют, по-видимому, о том, что удаление электрона из адсорбата активированным кислородом, удерживающимся на поверхности, является также довольно вероятным. Однако было показано, что после удаления всего кислорода восстановлением в водороде ЭПР-сигнал и образование катион-радикалов уменьшились, но не исключались полностью. [39]
 |
Константы СТВ изомерных бутенильных радикалов. [40] |
При облучении олефинов алкильные радикалы могут возникать: в результате присоединения атомов Н по двойной связи; при разрыве С - Н - связи; в результате присоединения молекулярного катиона к молекуле с образованием катион-радикала. Из спектра ЭПР часто трудно сделать однозначный вывод о природе алкильного радикала. [41]
Первая из трех волн на полярограмме перхлората 4 4 -фенил-бые - у у - ( 9 / 6) - дифенилпирилия при концентрации 1 - Ю 4 - 1 - 10 - 3 М соответствовала одноэлектронному процессу с образованием катион-радикала, а две другие - переносу второго электрона с образованием соединения хиноидной структуры. При низких концентрациях деполяризатора полярографическая картина может усложняться из-за образования ионных пар интермедиата с анионами фонового электролита. Исследованы фоновые соли с различными анионами, чтобы доказать их существенное влияние на морфологию вольтамперных кривых. [42]
На основании корреляции логарифмов констант скорости каталитического окисления бензола и алкилбензолов с соответствующими потенциалами ионизации и отсутствия кинетического изотопного эффекта в реакции толуолов ( CHgCgHg, CDgCgHg и CflgCgSg) сделан вывод о переносе электрона от субстрата к окислителю о образованием катион-радикала в лимитирующей стадии. [43]
Процессы типа ( 3.1, а) чаще всего предполагают простой разрыв связей, в отличие от второго механизма распада, который сопровождается перегруппировками с миграцией атомов водорода или ( реже) других фрагментов. Процессы образования менее стабильных катион-радикалов ( б) в совокупности с нейтральными частицами в некоторых случаях могут быть более энергетически выгодными, чем процессы образования более устойчивых катионов ( а) в сочетании с радикалами. Вследствие этого относительный вклад процессов типа ( 3.1 б) в общий ионный ток осколочных ионов приуменьшении энергии ионизации может возрастать. Этой особенностью фрагментации нередко пользуются для выявления пиков перегруппировочных ионов в спектрах. [44]
Считается, что в таком комплексе происходит активация кислорода на атомах кобальта с переносом заряда от Со2 кОа, Создается неравномерность в распределении заряда с донорны-ми участками Co2 s, на которых активируется RCHs. Проис - ходит образование катион-радикала КСНз, который, в свою очередь, реагирует с CV - с образованием гидропероксида. Последний быстро разлагается до альдегида и воды. [45]
Страницы: 1 2 3 4