Образование - надсерная кислота
Cтраница 1
Образование надсерной кислоты и иона персульфата происходит при электролизе водных растворов серной кислоты ( или сульфатов щелочных металлов) с гладким платиновым анодом при высоких плотностях тока. [1]
Образование надсерной кислоты в условиях электролиза за счет атомарного, кислорода, по-видимому, также не имеет места. Относительное содержание в воде, обогащенной тяже - H2SO4, HSO и SO - в серной кислоте лым изотопом кислорода разных концентраций; б - Зависимость О18, было показано, что пос - активности воды и удельной электропро-ле электролиза образовав - водности раствора H2SO4 от концентра-шийся персульфат калия не обогащается тяжелым изотопом кислорода. Это свидетельствует о том, что на аноде вероятнее всего происходит реакция непосредственного разряда анионов серной кислоты. [2]
Образование надсерной кислоты в условиях электролиза за счет атомарного кислорода, по-видимому, мало вероятно. Фрумкина и сотрудников [29] по электролизу раствора сульфата калия в воде, обогащенной тяжелым изотопом кислорода О18, было показано, что после электролиза образовавшийся персульфат калия не обогащается тяжелым изотопом кислорода. Это свидетельствует о том, что на аноде вероятнее всего происходит реакция непосредственного разряда анионов серной кислоты. [3]
Образование надсерной кислоты через перекись водорода следует признать маловероятным, поскольку активность воды в сильнокислых растворах резко понижена и разряд ее молекул едва ли возможен. За счет атомарного кислорода надсерная кислота образоваться, по-видимому, тоже не может. [4]
Образование надсерной кислоты в условиях электролиза за счет атомарного кислорода, по-видимому, также не имеет места. [5]
Механизм образования надсерной кислоты, предложенный Глесстоном и Хиклингом, следует признать маловероятным, так как в сильнокислых растворах, применяемых при электролизе и дающих наиболее высокие выходы надсерной кислоты, активность воды резко понижена и разряд молекул воды в значительных количествах едва ли возможен. Кроме того, платиновые аноды, которые только и применяются в ванных, являются очень сильными катализаторами распада перекиси водорода. [6]
В пользу образования надсерной кислоты из двух групп HSO4 говорит то обстоятельство, что выход, как будет более подробно-показано ниже, в разбавленных растворах очень мал и возрастает с увеличением Концентрации HjSOi. Дело в том, что в сильно-разбавленных растворах происходит диссоциация на ионы 2Н и SO4, в более концентрированных - на Н и HSOJ. Если в первом случае па аноде, в первую очередь, разряжаются ионы SCU дающие с водой серную кислоту и кислород, то во втором - ионы HSO, образующие падссрную кислоту. Поэтому образование помодней зависит не от количества ионов SO. Вопрос о том, является ли над серная кислота одно-ссповпой с формулой HSO /, или же двухосновной с соответствующей формулой НаБаОй, благодаря исследованиям Левенхерца, 7 - Брсдига 5 и Меллера Л7К решен в пользу двойной формулы. [7]
Однако равновесие реакции образования надсерной кислоты из серной и Н2Оц сильно сдвинуто в сторону получения монокадсерной кислоты. [8]
Предложено несколько электрохимических схем образования надсерной кислоты. [9]
На аноде наряду с образованием надсерной кислоты возможен разряд молекул воды, приводящий к выделению кислорода. [10]
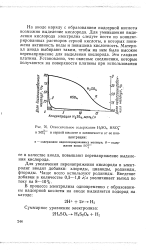 |
Относительное содержание H2SO4, HSO4. [11] |
На аноде наряду с образованием надсерной кислоты возможно выделение кислорода. Для уменьшения выделения кислорода электролиз следует вести из концентрированных растворов серной кислоты, в которых понижена активность воды и повышена кислотность. Материал анода выбирают таким, чтобы на нем было высокое перенапряжение для выделения кислорода. [12]
Получается в промышленности электролизом серной кислоты с образованием надсерной кислоты, термически разлагаемой на перекись водорода и серную кислоту. [13]
Таким образом, анодный распад мононадсерной кислоты тормозит образование надсерной кислоты и уменьшает выход ее по току. [14]
 |
Самодельный прибор Гофмана. [15] |
Страницы: 1 2 3