Образование - надсерная кислота
Cтраница 3
Особое значение при конструировании электролизеров для получения надсерной кислоты имеет высокая объемная плотность тока в анолите. Это необходимо для того, чтобы скорость образования мононадсерной кислоты и взаимодействия ее с анодом была во много раз меньше скорости образования надсерной кислоты. [31]
 |
Результаты опытов по изучению влияния температуры среды на очистку отработанной кислоты. [32] |
При прили-вании в такую кислоту перекиси водорода не наблюдалось вспенивания и реакция разложения Н2 02 шла очень медленно, в основном, вероятно, через образование надсерной кислоты. [33]
Другой способ понижения концентрации мононадсернои кислоты состоит в добавках к электролиту веществ, способствующих химическому разрушению мононадсернои кислоты, например небольших количеств соляной или сернистой ( 8Ог) кислоты. Добавка иона СГ, как и F -, влияет благоприятно также и в том отношении, что способствует повышению анодного потенциала, а это благоприятствует образованию надсерной кислоты. [34]
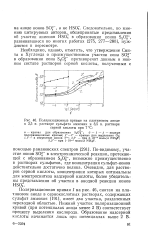 |
Поляризационные кривые на платиновом аноде. [35] |
Поляризационная кривая / на рис. 46, снятая на платиновом аноде в сернокислотных растворах, содержащих сульфат аммония [191], имеет два участка, разделенных переходной областью. Нижний участок поляризационной кривой ( при потенциалах анода менее 2 В) соответствует процессу выделения кислорода. Образование надсерной кислоты начинается лишь при потенциалах выше 2 В. [36]
Соответственное место гласит: Результаты Баха становятся понятными. Прибавляя перманганат известной концентрации к смеси перекиси водорода и серной кислоты, он думал, чго определяет концентрацию перекиси в растяоре. Но в действительности он употребил слишком мало перманганата, вследствие образования надсерной кислоты, и таким образом считал, что количество перекиси меньше, чем оно было в действительности. [37]
Отсюда совершенно необходимо, чтобы разложение по уравнению ( 3), являющееся следствием гидролиза надсерной кислоты до мононадссрной по уравнению ( 4), было бы по возможности устранено. Это может быть достигнуто выбором соответствующих условий процесса электролиза. Необходимо следить, чтобы при электролизе преобладали реакции ( 1), ( 2а) и ( 26), способствующие образованию надсерной кислоты, скорость же реакций от ( 3) до ( 7), протекающих как в электролите, так и на аноде и приводящих к уменьшению выхода надсерной кислоты, была бы по возможности мала. [38]
На рассматриваемом, участке электрохимические процессы подчиняются следующим закономерностям. Последнее обстоятельство является логичным следствием предлагаемой ниже схемы образования ( C1O4) 2S2O8, поскольку она предполагает потребление S2O8 - радикалов, образующихся при разряде ионов серной кислоты. Здесь следует добавить также, что ( C1O4) 2S2O8 получается в смеси электролитов в той области потенциалов, в которой в растворе, содержащем только серную кислоту, продолжается эффективное образование надсерной кислоты. [39]
Помутнение от азотнокислого серебра было при этом значительно слабее, чем вначале, и ие усиливалось от добавки сернокислого железа. С другой стороны, оно не было связано с изменением поверхности анода, так как при замене электролита чистой серной кислотой сразу же получались соответственно более низкие выходы по току. Незначительные количества азотной кислоты не влияют на образование надсерной кислоты. [40]
Образование ее нежелательно не только потому, что при разложении мононадсернои кислоты выделяется кислород, но и потому, что при этом происходит деполяризация анода. Снижение же потенциала анода приводит к уменьшению выхода надсерной кислоты. Количество мононадсернои кислоты увеличивается с повышением содержания HaSaOg, поэтому последняя может накапливаться лишь до определенного предела. Затем электролит подвергают гидролизу для выделения перекиси водорода, которую отгоняют и улавливают, а кубовый остаток возвращают на электролиз. Из этого следует, что содержание мононадсернои кислоты по сравнению с концентрацией надсерной кислоты необходимо поддерживать возможно более низким. Это обеспечивается увеличением плотности тока, благоприятствующим процессу образования надсерной кислоты. Содержание мононадсернои кислоты можно снизить также путем добавления к электролиту небольших количеств соляной или сернистой кислот, способствующих ее разложению. [41]
Страницы: 1 2 3